
| n |
| V |
| 36g |
| 136g |
| 9 |
| 34 |
| ||
| 34 |
| ||
| m |
| ρ |
| 221g-0.5mol×71g/mol-0.5mol×2g/mol |
| 1230g/L |
| 1mol |
| 0.15L |


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
| A、若M(甲)<M(乙),则分子数:甲<乙 |
| B、若M(甲)>M(乙),则气体摩尔体积:甲<乙 |
| C、若M(甲)<M(乙),则气体的压强:甲>乙 |
| D、若M(甲)<M(乙),则气体的体积:甲<乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
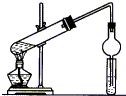 Ⅰ、某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%.
Ⅰ、某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%.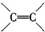
| 稀、冷KMnO4/OH- |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康或环境有很大影响 |
| B、福岛核电站泄漏的放射性物质131I和127I互为同位素,化学性质几乎相同 |
| C、在黑夜中,我们能看到一束汽车的灯光,是因为我们生活中的大气是胶体体系 |
| D、铝制品在空气中不易被腐蚀是因为铝的性质不活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①② | C、③④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl[NaCl] |
| B、CuCl2[CuCl2] |
| C、NaOH[NaOH] |
| D、CuSO4[Cu(OH)2] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A、反应开始20 s内,用二氧化氮表示的平均反应速率为0.0025 mol?L-1?s-1 |
| B、80s时混合气体的颜色与60s时的相同,比40 s时的颜色深 |
| C、80s时向容器中再加入0.32 mol氮气,同时将容器扩大为4L,则平衡不移动 |
| D、保持其他条件不变,起始时向容器中充入0.20 mol N2O4,达平衡时各物质含量与原平衡相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com