
| A. | 一氯甲烷的结构式:CH3Cl | B. | 苯的分子式: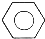 | ||
| C. | 葡萄糖的结构简式:C6H12O6 | D. | 丙烷分子的球棍模型: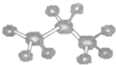 |
分析 A.结构式中含C-H、C-Cl;
B.1个苯分子中含6个C、6个H;
C.结构简式中体现官能团;
D.丙烷中甲基、亚甲基均为四面体构型,由球表示原子,棍表示化学键.
解答 解:A.一氯甲烷的结构间式为CH3Cl,一氯甲烷的结构式是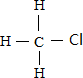 ,故A错误;
,故A错误;
B.苯的分子式为C6H6,结构简式为 ,故B错误;
,故B错误;
C.葡萄糖的分子式为C6H12O6,结构简式为CH2OH(CHOH)4CHO,故C错误;
D.丙烷分子的球棍模型为 ,故D正确;
,故D正确;
故选D.
点评 本题考查化学用语,涉及电子式、结构式、结构简式、球棍模型等,为高频考点,把握化学用语的区别及规范使用为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 该有机物分子式为C11H12O6 | |
| B. | 分子中最多有10个碳原子共平面 | |
| C. | 1 mol该有机物分别与足量NaOH溶液、NaHCO3溶液完全反应,消耗NaOH、NaHCO3的物质的量分别为4mol、1 mol | |
| D. | 该有机物可发生取代反应、还原反应,不能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
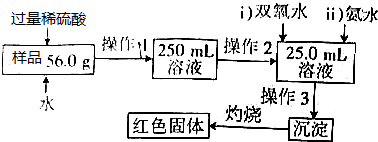
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质序号 | 被提纯物(杂质) | 试剂 | 分离方法 |
| ① | CH3CH3(CH2=CH2) | ||
| ② | CH2=CH2(SO2) | ||
| ③ | 乙酸乙酯(乙酸) | ||
| ④ | 乙醇(水) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
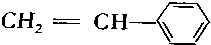
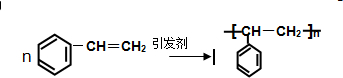 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取溶解后待测液少许,先加少量氯水,再加KSCN产生血红色溶液,则有Fe2+ | |
| B. | 步骤3的离子方程式为:5C2O42-+2MnO${\;}_{4}^{-}$+8H2O=10CO2↑+2Mn2++16OH- | |
| C. | x:z=1:2 | |
| D. | 该晶体的化学式为:K3[Fe(C2O4)3]•3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)2 | B. | NaOH | C. | NaHCO3 | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHS在水中的电离方程式为:NaHS═Na++H++S2- | |
| B. | 已知某温度下Ksp(CH3COOAg)=2.8×10-3,此温度下浓度均为0.1 mol•L-1的AgNO3溶液和CH3COONa溶液等体积混合一定能产生CH3COOAg沉淀 | |
| C. | 0.1mol/L CH3COOH溶液与0.05mol/L NaOH溶液等体积混合,所得溶液中:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) | |
| D. | 0.2mol/LNH3•H2O溶液与0.1mol/L盐酸等体积混合后,溶液显碱性,则:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com