


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
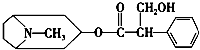 中国科学家从中药材中提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有良好的治愈率,从而在防治禽流感药物研究方面取得重大突破.已知金丝桃素的结构简式如图所示,下列有关说法正确的是( )
中国科学家从中药材中提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有良好的治愈率,从而在防治禽流感药物研究方面取得重大突破.已知金丝桃素的结构简式如图所示,下列有关说法正确的是( )| A、金丝桃素的分子式为C17H22O3N |
| B、金丝桃素能在NaOH溶液中加热反应得到两种芳香族化合物 |
| C、在加热条件下金丝桃素能与浓硫酸和浓硝酸的混合液发生取代反应 |
| D、1mol金丝桃素最多能与4mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.8g苯中含有0.3NA个碳碳双键,0.3NA个碳碳单键 |
| B、2L 0.1 mol/L的醋酸钠溶液中,醋酸根离子数为0.2NA |
| C、5.6g铁与足量的稀硝酸反应,失去电子数为0.2NA |
| D、SiO2晶体中,有NA个Si就有4NA个Si-O键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、贝采利乌斯 | B、维勒 |
| C、李比希 | D、海维西 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com