
【题目】向体积为2 L的固定密闭容器中通入3 mol X气体,在一定温度下发生如下反应:2X(g)![]() Y(g)+3Z(g)。
Y(g)+3Z(g)。
(1)经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的速率为________ mol·L-1·min-1。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为 甲:v(X)=3.5 mol·L-1·min-1; 乙:v(Y)=2 mol·L-1·min-1;丙:v(Z)=4.5 mol·L-1·min-1; 丁:v(X)=0.075 mol·L-1·s-1。若其他条件相同,温度不同,则温度由高到低的顺序是(填序号)________。

(3)若向达到(1)的平衡体系中充入氦气,则平衡______(填“向左”、“向右”或“不”)移动;若从达到(1)的平衡体系中移走部分Y气体,则平衡________(填“向左”、“向右”或“不”)移动。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5 mol X气体,则平衡后X的转化率与(1)的平衡中X的转化率相比较________。
A.无法确定 B.前者一定大于后者 C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,则:a、b、c应该满足的关系为_____________________________。
【答案】 0.03 丁>乙>甲>丙 不 向右 B c=3b,a≥0
【解析】(1)设X物质的量的变化量是x,则
2X(g)Y(g)+3Z(g)
初始物质的量:3 0 0
变化物质的量:x 0.5x 1.5x
平衡物质的量:3-x0.5x 1.5x
经5min后达平衡,此时容器内压强为起始时的1.2倍,即![]() =
=![]() ,解得x=0.6mol,所以Y的物质的量变化量是0.3mol,表示的化学反应速率为:
,解得x=0.6mol,所以Y的物质的量变化量是0.3mol,表示的化学反应速率为:![]() =0.03mol/(Lmin),故答案为:0.03;
=0.03mol/(Lmin),故答案为:0.03;
(2)将四个反应速率甲:ν(X)=3.5mol/(Lmin);乙:ν(Y)=2mol/(Lmin);丙:ν(Z)=4.5mol/(Lmin);丁:ν(X)=0.075mol/(Ls),都统一到用X表示的反应速率值分别为甲:ν(X)=3.5mol/(Lmin);乙:ν(X)=4mol/(Lmin);丙:ν(X)=3mol/(Lmin);丁:ν(X)=4.5mol/(Lmin),所以化学反应速率是丁>乙>甲>丙,温度越高,化学反应速率越快,所以温度大小关系是:丁>乙>甲>丙,故答案为:丁>乙>甲>丙;
(3)若向达到(1)的平衡体系中充入氮气,不会改变各组分的浓度,所以平衡不会移动,若将达到(1)的平衡体系中移走部分混合气体,则体系压强会减小,所以平衡向着气体系数和增大的方向进行,即向着正方向进行,故答案为:不;向右;
(4)若在相同条件下向达到(1)所述平衡体系中再充入0.5molX气体,则体系压强增大,新平衡相当于是在原平衡基础上增大压强,平衡逆向移动,所以平衡后X的转化率减小,故答案为:B;
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达平衡时仍与(1)的平衡等效,根据极限转化结构以及等效的条件,需要等比即等效,即
2X(g)Y(g)+3Z(g)
(1)的投料:3mol 0 0
等效投料: 0 1.5mol 4.5mol,
现在投料: a b c
等效投料: 0 0.5a+b1.5a+c
所以![]() =
=![]() ,解得c=3b,且a≥0,故答案为:c=3b,a≥0。
,解得c=3b,且a≥0,故答案为:c=3b,a≥0。


科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性。常温下,0.1 molL-1 t溶液与0.1 molL-1 u溶液的pH 均为1。下列说法不正确的是
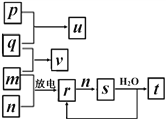
A. Y、W的最高价氧化物对应的水化物均为强酸
B. 元素的非金属性:Z>Y>X,原子半径:X<Z<Y
C. s溶于水的反应中,氧化剂与还原剂的物质的量之比为1:2
D. v的电子式可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用SNCR脱硝技术的原理是4NO(g)+4NH3(g)![]() 4N2(g)+6H2O(g),下图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是( )
4N2(g)+6H2O(g),下图是其在密闭体系中研究反应条件对烟气脱硝效率的实验结果。下列说法正确的是( )
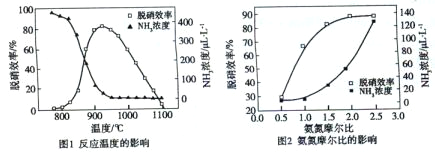
A. 从图1判断,该反应的正反应方向是放热反应
B. 从图2判断,减少氨气的浓度有助于提高NO的转化率
C. 从图1判断,脱硝的最佳温度约为 925℃
D. 从图2判断,综合考虑脱硝效率和运行成本最佳氨氮摩尔比应为2.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕集、利用与封存是我国能源领域的一个重要战略方向,发展成一项重要的新兴产业。
(1)已知:CH4、CO、H2的燃烧热分别为890kJmol-1、283kJmol-1、285.8kJmol-1,计算下列反应的反应热。CO2(g)+CH4(g)=2CO(g)+ 2H2(g)ΔH=___________kJmol-1。
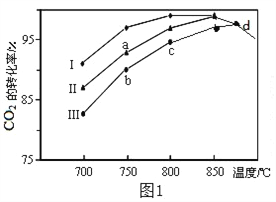
(2)利用废气中的CO2为原料制取甲醇,反应方程式为:CO2+3H2![]() CH3OH+H2O其他条件相同,该甲醇合成反应在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下反应相同时间后,CO2的转化率随反应温度的变化如图1所示。
CH3OH+H2O其他条件相同,该甲醇合成反应在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下反应相同时间后,CO2的转化率随反应温度的变化如图1所示。
①该反应的ΔH_____0(填“>”或“<”)
②d点不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下CO2的转化率相同的原因是________。
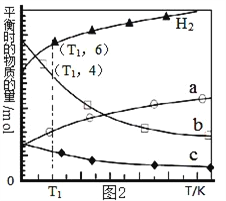
(3)用二氧化碳催化加氢来合成低碳烯烃,起始时以0.1MPa,n(H2)∶n(CO2)=3∶1的投料比充入反应器中,发生反应:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g)△H,不同温度下平衡时的四种气态物质的物质的量如图2所示:
C2H4(g)+4H2O(g)△H,不同温度下平衡时的四种气态物质的物质的量如图2所示:
①该反应在_________自发进行(填“低温”或“高温”)。
②b代表的物质是______________。
③T1温度下的平衡转化率为_________________,相对于起始状态,平衡时气体的平均分子量增大的百分率为______________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙酸乙酯(C4H8O2)是一种无色液体,不溶于水,密度小于1 g·mL-1,沸点约为55 ℃。要从水与乙酸乙酯的混合物中将乙酸乙酯分离出来,下列方法中最简便的是
A.蒸馏B.分液C.过滤D.蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,已知A元素的最低化合价为-3价,它的最高价氧化物含氧56.21%,原子核内中子数比质子数多1,试回答(均用具体的元素符号或化学式回答):
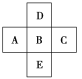
(1)写出它们的元素符号:A________,B________,C________,D________。
(2)A、B、C、D的气态氢化物稳定性最差的是________。
(3)A、B、C的原子半径由小到大的顺序是________。
(4)A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com