
【题目】如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是()
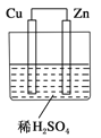
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42-向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu→Zn
⑥正极反应式:Cu+2e-==Cu2+,发生氧化反应
A. ①②③B. ②④C. ②③④D. ③④⑤⑥
【答案】B
【解析】
Zn和Cu形成的原电池中,活泼金属Zn是负极,不活泼金属Cu是正极,Zn片上Zn失电子发生氧化反应,Cu片上H+得电子发生还原反应,电子由负极经导线流向正极,阳离子移向正极,阴离子移向负极。
①在Zn和Cu形成的原电池中,由于金属活动性Zn>Cu,所以Zn是负极,Cu是正极,故错误;
②铜电极上H+得电子发生还原反应,电极反应式为2H++2e-=H2↑,故正确;
③阴离子移向负极,则硫酸根离子向负极锌移动,故错误;
④若有0.5mol电子流经导线,由电极反应式2H++2e-=H2↑可知产生气体的物质的量为0.25mol,故正确;
⑤电子由负极经导线流向正极,则电子由Zn电极流向Cu电极,故错误;
⑥铜电极上H+得电子发生还原反应,电极反应式为2H++2e-=H2↑,故错误;
②④正确,故选B。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 液溴易挥发,在存放液溴的试剂瓶中应加水封
B. 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
C. 某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-
D. 某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R、I、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,I的原子序数是W的两倍,Q的最外层只有一个电子,其他电子层电子均处于饱和状态.请回答下列问题:
(1)Q+核外电子排布式为___________,Y的电子排布图为_________________________
(2)化合物ZX3中Z原子的杂化方式为___________,ZW2- 离子的立体构型是___________;
(3)①Y、R的最高价氧化物的沸点较高的是___________(填化学式),原因是___________;
②W与I的简单氢化物中W的熔沸点更高,原因是______________________
(4)向Q元素的硫酸盐溶液中通入足量ZX3,充分反应后溶液呈深蓝色,该反应的离子方程式为__________________________________________________;
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为___________,Y原子的配位数为___________,若晶胞的边长为a pm,晶体的密度为ρ g/cm3,则阿伏加德罗常数的数值为___________(用含a和ρ的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是“化学元素周期表国际年”,有关118号元素295Og说法错误的是( )
A.原子核外电子数为118B.是零族元素
C.位于第六周期D.原子的质量数为295
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL溴化亚铁溶液中通入2.24L氯气(标准状况),若有三分之一的溴离子被氧化,则原溴化亚铁溶液的物质的量浓度为( )
A. 3mol/L B. 1. 2mol/L
C. 1. 5mol/L D. 2.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物 A——G之间存在如下转化关系,除D以外其他物质均为芳香族化合物,其中化合物B分子中含有一个甲基,化合物D完全燃烧生成等物质的量的CO2 和H2O ,且D蒸汽与氢气的相对密度为30。回答下列问题:
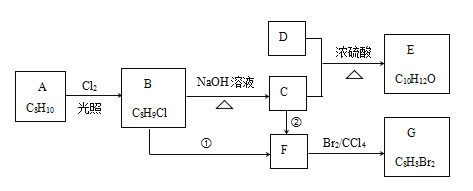
(1)化合物A的名称__________________,化合物D的分子式为_____________。
(2)① 的反应类型为 _____________。
② 需要的试剂和反应条件是______________________。
(3)C中含氧官能团的名称为___________。F的结构简式为___________。
(4)C + D![]() E的化学方程式为_____________________。
E的化学方程式为_____________________。
(5)同时符合下列条件的E的同分异构体有_____种,其中分子中有五种不同化学环境的氢,数目比为1:1:2:2:6 的结构简式为________________。
①苯环上有两个侧链 ②分子中含有两个甲基
③能发生水解反应且水解产物能使氯化铁溶液显紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯: 6 H2(g) +2CO2(g)![]() CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
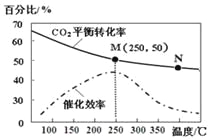
A. 生成乙烯的速率:v(M)一定小于v(N)
B. 化学平衡常数:KN>K M
C. 当温度高于250℃时,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低
D. 若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com