
| A | B | C | D | |
| 强电解质 | NaCl | H2SO4 | CaCO3 | HNO3 |
| 弱电解质 | HF | BaSO4 | HClO | CH3COOH |
| 非电解质 | Cl2 | CO2 | C2H5OH | H2O |
| A、A | B、B | C、C | D、D |


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
| A、干馏煤可以得到甲烷、苯和氨等重要化工原料 |
| B、用于奥运“祥云”火炬的丙烷是一种清洁燃料 |
| C、乙醇和乙酸都能发生氧化反应 |
| D、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸 | B、氢氧化钠 |
| C、氨气 | D、氯化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(B2)=0.8mol?L-1?s-1 |
| B、v(A2)=0.4mol?L-1?s-1 |
| C、v(C)=0.6mol?L-1?s-1 |
| D、v(B2)=42mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素A、B、C、D在周期表中位置如图所示,其中元素D原子最外层有3个电子.
短周期元素A、B、C、D在周期表中位置如图所示,其中元素D原子最外层有3个电子.| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1,2,3,-三甲基苯 |
| B、丙烷 |
| C、异丙醇 |
| D、甲酸丁酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
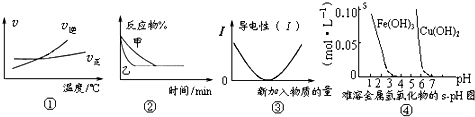
| A、根据图①可判断可逆反应“A2(g)+3B2(g)?2AB3(g)”的△H>0 |
| B、图②表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
| C、图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D、根据图④,若要除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO,至pH=4左右 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、MnO2作氧化剂,发生氧化反应 |
| B、在反应中,表现还原性与表现酸性的HCl的物质的量之比为2:1 |
| C、每生成1mol Cl2时,有4mol电子发生转移 |
| D、氧化性:MnO2>Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com