
月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为________。
(2)Na的原子结构示意图为________,Na在氧气中完全燃烧所得产物的电子式为________。
(3)MgCl在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点________(填“高”或“低”)。
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为__________________________;SiO2的晶体类型为________。
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为________________(写化学式)。
(4)月壤中含有丰富的3He,从月壤中提炼1 kg 3He,同时可得6000 kg H2和700 kg N2,若以所得H2和N2为原料经一系列反应最多可生产碳酸氢铵________kg。
[答案] (1)1 (2)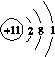

(3)①高 ②SiO2+2OH-===SiO +H2O 原子晶体 ③NaCl,NaClO,Na2CO3
+H2O 原子晶体 ③NaCl,NaClO,Na2CO3
(4)3950
[解析] (3)①离子晶体的熔点与晶格能有关系,形成离子键的离子半径越小,离子所带电荷数越多,离子键越强,晶格能越大,熔点越高;镁离子的半径小于钡离子,故氧化镁的晶格能大于氧化钡的晶格能,则氧化镁的熔点高;②氧化镁是碱性氧化物,二氧化硅是酸性氧化物,可用强碱溶液除去二氧化硅;二氧化硅是由硅原子和氧原子通过共价键形成的空间网状结构的晶体,是原子晶体;③氧化镁、炭粉和氯气制备氯化镁,另一生成物可被氢氧化钠完全吸收,则生成气体是二氧化碳,它与足量氢氧化钠反应生成碳酸钠,过量的氯气与氢氧化钠反应生成氯化钠和次氯酸钠。(4)根据化学方程式3H2+N2 2NH3,结合已知可知N2不足,则最多生成的NH3的物质的量为
2NH3,结合已知可知N2不足,则最多生成的NH3的物质的量为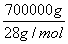 ×2,根据氮原子守恒可知最终生成碳酸氢铵的质量为
×2,根据氮原子守恒可知最终生成碳酸氢铵的质量为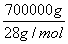 ×2×79 g·mol-1=3 950 000 g=3950 kg。
×2×79 g·mol-1=3 950 000 g=3950 kg。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
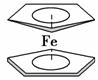 二茂铁分子[Fe(C5H5)2]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右图所示,下列说法正确的是
二茂铁分子[Fe(C5H5)2]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右图所示,下列说法正确的是
A.二茂铁中Fe2+与环戊二烯离子(C5H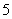 )之间为离子键
)之间为离子键
B.Fe元素在周期表中的位置是第四周期ⅧA
C.Fe2+的电子排布式为1s22s22p63s23p63d6
D.环戊二烯( )中的碳原子有sp杂化、sp2杂化、sp3杂化
)中的碳原子有sp杂化、sp2杂化、sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是( )
A.原子最外层电子数:X>Y>Z
B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z-
D.原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式:__________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为__________,其水溶液与F单质反应的化学方程式为____________________________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显______色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为______________;c的电子式为________;d的晶体类型是________。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是
A. Th 元素的质量数是232 B. Th 元素的相对原子质量是231
C. 232Th 转换成233U是化学变化 D. 230Th和232Th的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
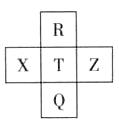 元素R、X、T、Z、Q在元素周期表
元素R、X、T、Z、Q在元素周期表 中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
A.非金属性:Z<T<X
B.R与Q的电子数相差26
C.气态氢化物稳定性:R <T<Q
D.最高价氧化物的水化物的酸性:T>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
按下列实验方法制备气体,合理而又实用的是( )
A.锌粒与稀硝酸反应制备H2
B.将饱和氨水滴加到新制的生石灰制NH3
C.亚硫酸钠与浓硫酸反应制备SO2
D.大理石与浓硫酸反应制备CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的核外电子排布式______________________________________。
(2)CoTiO3晶体结构模型如图1所示。在CoTiO3晶体中1个Ti原子、1个Co原子,周围距离最近的O原子数目分别为________个、________个。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO-互为等电子体的分子、离子化学式分别为________、________(各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图2所示。
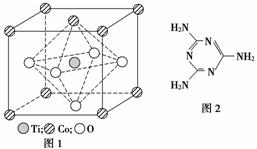
三聚氰胺分子中氮原子轨道杂化类型是________,1 mol三聚氰胺分子中σ键的数目为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com