
【题目】有关物质的转化关系如下图所示(部分物质和条件已经略去)。已知D是化学实验室中常见的淡黄色固体,B、C为常见气体单质,F是常见的液体;K是肉类食品常用的食品添加剂。

请回答下列问题:
(1)D的电子式为_____________。
(2)H的化学式为_____________。
(3)写出反应①的化学方程式:__________________________________________;
(4)写出反应②的离子方程式:__________________________________________。
【答案】![]() NH3 4NH3 + 5O2
NH3 4NH3 + 5O2 ![]() 4NO + 6H2O NO + NO2 +2OH一
4NO + 6H2O NO + NO2 +2OH一 ![]() 2 NO2一 + H2O
2 NO2一 + H2O
【解析】
D是化学实验室中常见的淡黄色固体,则D为Na2O2,F是常见的液体,则F为H2O,Na2O2与H2O反应生成NaOH和O2,C为常见气体单质,则C为O2,G为NaOH,K是肉类食品常用的食品添加剂,则K为NaNO2,其中的N元素由B提供,B为常见气体单质,则B为N2,A(Na)与B(N2)反应生成C(NaN3),则C为NaN3,NaN3与F(H2O)反应生成氨气和G(氢氧化钠),则H为NH3,NH3与C(O2)反应生成一氧化氮和水,则I为NO,NO与氧气反应生成NO2,则J为NO2,NO、NO2与NaOH反应生成NaNO2和水,据此答题。
(1)D为Na2O2,Na2O2中既含离子键又含共价键,电子式为![]() ,故答案为:
,故答案为:![]() 。
。
(2)H为氨气,化学式为NH3,故答案为:NH3。
(3)反应①为氨气在催化剂的条件下与氧气反应生成一氧化氮和水,化学方程式为:4NH3 +5O2![]() 4NO+6H2O,故答案为:4NH3 +5O2
4NO+6H2O,故答案为:4NH3 +5O2![]() 4NO+6H2O。
4NO+6H2O。
(4)反应②为NO、NO2与NaOH反应生成NaNO2和水,化学方程式为NO+NO2+2NaOH=2NaNO2+H2O,离子方程式为:NO +NO2+2OH-![]() 2NO2-+H2O,故答案为:NO+NO2+2OH-
2NO2-+H2O,故答案为:NO+NO2+2OH-![]() 2NO2-+H2O。
2NO2-+H2O。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是取样,先滴加KSCN溶液,再滴加____,该过程的现象为__________________________________________________。
(2)步骤②加入过量H2O2的目的是___________________________________。
(3)步骤③中反应的离子方程式是__________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、____________、灼烧、______、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应总伴随着能量的变化,下列叙述中正确的是
A.图1表示25min内,Y的平均速率为0.016molL-1min-1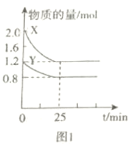
B.图2可表示碳与二氧化碳的反应能量变化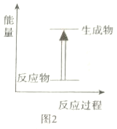
C.图3表示在铁金属内部电子流向碳一侧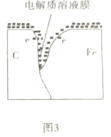
D.图4表示反应2NO+2CO=N2+2CO2中NO和CO转化率为2:1时,反应达平衡状态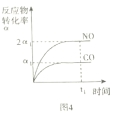
查看答案和解析>>
科目:高中化学 来源: 题型:
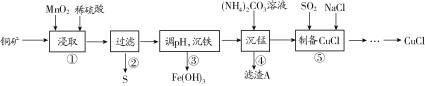
【题目】用某铜矿(含CuS以及少量FeO和Fe2O3)制备CuCl的主要流程如下:
已知Fe3+、Mn2+、Cu2+生成氢氧化物沉淀时的pH如下表所示:
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Mn(OH)2 | 7.1 | 10.1 |
Cu(OH)2 | 4.7 | 6.7 |
(1)浸取时,CuS被浸取的离子方程式为CuS+MnO2+4H+=Cu2++Mn2++S↓+2H2O,该反应的氧化剂是________(填化学式),Fe2O3被浸取的离子方程式为________________。
(2)步骤③调整pH的范围为______,滤渣A的成分为________(填化学式)。
(3)“沉铁”时,需要检验Fe3+是否沉淀完全,所用的试剂为________(填化学式)。
(4)准确称取所制备的氯化亚铜样品1.600 g,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用0.100 0 mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液25.00 mL,反应中Cr2O72-被还原为Cr3+,计算样品中CuCl的质量分数(写出计算过程)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是
图1 图2
图2
A. 选择合适的试剂,用图1所示装置可制取和收集少量CO2、NO和O2
B. 实验室制备氢氧化铝时,可向硫酸铝溶液中逐滴加入稀氨水
C. 可用图 2装置分离碘和四氯化碳溶液
D. 配制100mL 0.1 mol/L NaCl溶液时,用托盘天平准确称取NaCl固体5.85g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面列出了几组物质:A.金刚石与石墨;B.丙烯与环丙烷;C.氕与氘;D.甲烷与戊烷;E.液氨与氨水;F. ![]() 与
与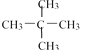 ;G.
;G. 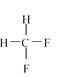 与
与 ,请将物质的合适组号填写在空格上。
,请将物质的合适组号填写在空格上。
①同位素_________
②同素异形体_________
③同系物_________
④同分异构体_________
⑤同一物质_________。
(2)下列物质中:①Ar ②MgBr2 ③Na2O2 ④H2SO4 ⑤CS2 ⑥NH4Br ⑦BaO ⑧RbOH。只存在共价键的是_________ (填序号,下同),只存在离子键的是_________,既存在离子键又存在极性共价键的是_________,既存在离子键又存在非极性共价键的是_________。
(3)异丁烷的一氯代物有_________种,新戊烷的一氯代物有_________种。C3H2Cl6的同分异构体有_________种,C5HCl11的同分异构体有_________种,乙烷和氯气在光照条件下发生取代反应所得产物最多有_________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学和环境保护、食品营养、材料应用等密切相关。
(1)防治环境污染、改善生态环境已成为全人类的共识。
①下列各项中,完成空气质量报告时不需要监测的是______(填字母)。
a.二氧化碳的浓度 b.二氧化硫的浓度 c.可吸入颗粒物的浓度
②下列做法中不利于改善环境质量的是________(填字母)。
a.将废旧电池进行深埋处理
b.充分利用风能等新能源
c.给汽车加装尾气催化净化装置
③工业废水需处理达标后才能排放。轧钢厂排出的废水主要是含盐酸的酸性废水,处理此废水可采用的方法是______(填字母)。
a.氧化还原法 b.中和法 c.沉淀法
(2)营养平衡、合理用药是保证人体健康和生活质量的重要途径。
①在氢、钠、铁这三种元素中,属于人体生命活动必需微量元素的是______(填元素符号)。
②下列物质中,具有抗菌消炎疗效的是________(填字母)。
a.氨基酸 b.阿斯匹林 c.青霉素
③如图为某品牌鸡精标签的一部分,其中能水解生成氨基酸的配料是________,属于着色剂的是__________,属于防腐剂的是________。

(3)材料是人类社会发展的物质基础,材料科学的发展离不开化学。
①水泥、玻璃及陶瓷都是传统的硅酸盐材料,生产水泥和玻璃都用到的原料是________;蓝色玻璃是在其中添加了氧化物________(写化学式);SiC是一种新型的陶瓷,工业上用石英砂与焦炭高温条件下生成SiC的同时的生成CO,该制备反应的化学方程式为_____________。
②钢铁制品在潮湿的空气中发生______(填“化学”或“电化学”)腐蚀是造成钢铁腐蚀的主要原因。硬铝(一种铝合金)是制造飞机和宇宙飞船的理想材料,和纯铝相比,硬铝强度________________(填“低”“高”或“无法确定”),具有较强的抗腐蚀能力。
③橡胶是制造轮胎的重要原料,天然橡胶通过________(填“硫化”“氧化”或“老化”)措施可增大其强度、弹性和化学稳定性等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于取代反应的是
A. CH2=CH2 + H2O![]() CH3CH2OH
CH3CH2OH
B. ![]() +Br2
+Br2![]()
![]() +HBr
+HBr
C. 2CH3CH2OH![]() C2H5—O—C2H5 + H2O
C2H5—O—C2H5 + H2O
D. ![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量的蔗糖(C12H22O11)放入烧杯中,滴入几滴水并搅拌均匀,然后再加入适量的浓硫酸,迅速搅拌,放出大量的热,同时观察到固体逐渐变黑。片刻后,黑色物质急剧膨胀,并产生大量刺激性气味的气体(实验过程如图所示)
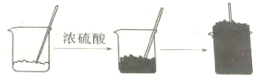
(1)固体变黑体现了浓硫酸的__________性。
(2)为了确定刺激性气味气体的成分,收集性所得气体,分别进行如下实验。
①将气体通入品红溶液后,溶液褪色,加热,颜色恢复。说明该气体中一定含有_________。
②将气体通入澄清石灰水,溶液变浑浊,_________(填“能”或“不能”)证明气体中含有CO2,其理由为______(用离子方程式表示)。
③刺激性气味气体产生的原因可用化学方程式表示为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com