
根据化学方程式回答下列问题
Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(1)该反应中H2SO4既起了氧化剂的作用,又起了________作用。
(2)若生成32gSO2被还原的H2SO4是________g。
(3)若用该方法制取定量的CuSO4时,有两个缺点:一是________,二是________________。解决这两个缺点的方法是:先将Cu与________反应,再与________反应。
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:阅读理解
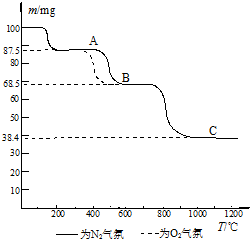
查看答案和解析>>
科目:高中化学 来源: 题型:



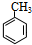



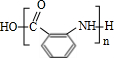

 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 的流程图.
的流程图.
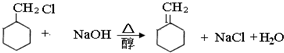

查看答案和解析>>
科目:高中化学 来源: 题型:
 的物质,该物质是一种香料.
的物质,该物质是一种香料.


 或
或
 或
或


 的水解产物
的水解产物 不能经氧化反应⑥得到产品
不能经氧化反应⑥得到产品 的水解产物
的水解产物 不能经氧化反应⑥得到产品
不能经氧化反应⑥得到产品查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com