

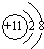 ,故答案为:第三周期第ⅥA族;
,故答案为:第三周期第ⅥA族;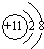 ;
; ,故答案为:
,故答案为: ;
;
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| △ |
| ||
| △ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3种 | B、4种 | C、5种 | D、6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D | E |
| 性质 或结 构信 息 | 室温下单质呈气态,原子最外层电子数与D相同 | D3B中阳离子与阴离子的电子层结构相同 | A和C可形成两种常见的化合物甲和乙,甲有强氧化性 | 单质质软、银白色固体、导电性强,在空气中燃烧生成淡黄色固体 | E的气态氢化物和最高价氧化物对应的水化物均为强酸,C、D和E三种元素形成的一种盐丙为某消毒液的主要成分 |
| 酸 | 电离常数 |
| HClO | Ka=3.0×10-8 |
| H2CO3 | Ka1=4.3×10-7,Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 还原 |
| ①NaCN |
| ②H+ |
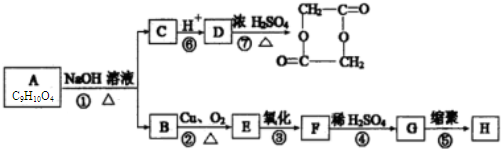

查看答案和解析>>
科目:高中化学 来源: 题型:
 “人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简
“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简| A、遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 |
| B、滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C、该分子中的所有碳原子不可能共平面 |
| D、1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是放热反应都是自发的,吸热反应都是非自发的 |
| B、自发反应一定是△S>0,非自发反应一定是△S<0 |
| C、△S>0且放热的反应一定是自发反应 |
| D、非自发反应在任何条件下都不能实现 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com