
����Ŀ���л��ϳ���ҩ��ҵ�е���Ҫ�ֶΡ�G��ij����֢ҩ����м��壬��ϳ�·�����£�

��֪��
 �����л�ԭ�ԣ����ױ���������
�����л�ԭ�ԣ����ױ���������
��1��B�Ľṹ��ʽΪ ______��
��2����Ӧ�ܵ�����Ϊ ___________ ���ٵķ�Ӧ����Ϊ ____________ ����Ӧ�ڵ�������_________ ��
��3�����ж��л���G�������Ʋ���ȷ���� __________����ѡ����ĸ����
A���������ԣ��������ᷴӦҲ����Ӧ
B���ܷ�����ȥ��Ӧ��ȡ����Ӧ��������Ӧ
C���ܾۺϳɸ߷��ӻ�����
D��1molG������NaHCO3��Һ��Ӧ�ų�2molCO2
��4��D��������NaHCO3��Һ��Ӧ�Ļ�ѧ����ʽΪ_______��
��5����������������C��ͬ���칹���� _____�֡�
A�����ڷ����廯����Һ���������
B���ܷ���������Ӧ
C����FeCI3��Һ������ɫ��Ӧ
���к˴Ź���������4��壬�ҷ����֮��Ϊ6��2��2��1����___��д������һ�ֽṹ��ʽ��
��6����֪����������������ʱ���������ȡ�������ڱ������ڶ�λ���������з��ʱ���������ȡ�������ڱ�һƽ�ļ�λ���������е���Ϣ��д���Լױ�Ϊԭ�Ϻϳ��л��![]() ��������ͼ�����Լ���ѡ��________���ϳ�·������ͼʾ�����£�
��������ͼ�����Լ���ѡ��________���ϳ�·������ͼʾ�����£� ![]() Ŀ����
Ŀ����
���𰸡� ��![]() Ũ���ᡢŨ���ᡢ���� ȡ����Ӧ ������������Է������� C
Ũ���ᡢŨ���ᡢ���� ȡ����Ӧ ������������Է������� C  16
16 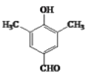 ��
��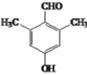

��������C����������Ӧ����D����D�Ľṹ��������֪CΪ![]() ��A��B��Ӧ����C�����B�ķ���ʽ������ķ�Ӧ��Ϣ����֪BΪ
��A��B��Ӧ����C�����B�ķ���ʽ������ķ�Ӧ��Ϣ����֪BΪ![]() ��AΪ
��AΪ![]() ��D����ˮ�ⷴӦ���ữ�õ�EΪ
��D����ˮ�ⷴӦ���ữ�õ�EΪ![]() ����G�Ľṹ��ʽ��֪��E����������Ӧ����F
����G�Ľṹ��ʽ��֪��E����������Ӧ����F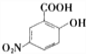 ��F�ٷ�����ԭ��Ӧ�õ�G��
��F�ٷ�����ԭ��Ӧ�õ�G��
��1��������������֪��B�Ľṹ��ʽΪ��![]() ,�ʴ�Ϊ��
,�ʴ�Ϊ��![]() ��
��
��2����Ӧ��Ϊ������Ӧ����Ӧ����Ϊ��Ũ���ᡢŨ���ᡢ���ȣ����ķ�Ӧ����Ϊȡ����Ӧ����Ӧ���������DZ������ǻ����Է���������
�ʴ�Ϊ��Ũ���ᡢŨ���ᡢ���ȣ�ȡ����Ӧ���������ǻ����Է���������
��3��A��G���а������Ȼ����������ԣ��������ᷴӦҲ�ܺͼӦ����A��ȷ��B��G���ܷ�����ȥ��Ӧ����B����C�������Ȼ����������ܽ������ۣ��γɸ߷��ӻ������C��ȷ��D���Ȼ�����NaHCO3��Ӧ����CO2��1molG������NaHCO3��Һ��Ӧ�ų�1molCO2����D��������ѡAC��
��4��D���Ȼ���ˮ��õ���������ǻ�����NaOH��Ӧ����Ӧ��ѧ����ʽΪ��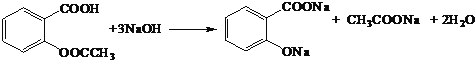 ��
��
��5��CΪ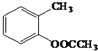 ,��������������C��ͬ���칹�壺a�����ڷ����廯�������Һ�����������˵�����б�����2��CH3��b���ܷ���������Ӧ��˵������CHO��c����FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ����������ĸ�ȡ������2��CH3��1��OH��1��CHO��
,��������������C��ͬ���칹�壺a�����ڷ����廯�������Һ�����������˵�����б�����2��CH3��b���ܷ���������Ӧ��˵������CHO��c����FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ����������ĸ�ȡ������2��CH3��1��OH��1��CHO��
����Ϊ![]() ������Hԭ�ӱ�OH��CHOȡ������OH��
������Hԭ�ӱ�OH��CHOȡ������OH�� ��1��λ�ã�-CHO��3��λ�ã���-OH��2��λ�ã�CHO��3�֡�3��λ�����ʹ�6��ͬ���칹����
��1��λ�ã�-CHO��3��λ�ã���-OH��2��λ�ã�CHO��3�֡�3��λ�����ʹ�6��ͬ���칹����
����Ϊ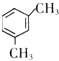 ������Hԭ�ӱ�OH��CHOȡ������OH��
������Hԭ�ӱ�OH��CHOȡ������OH�� ��1��λ�ã�-CHO��2��λ�ã���-OH��2��λ�ã�-CHO��2��λ�ã���-OH��3��λ�ã�-CHO��3��λ�ã���7��ͬ���칹�壻����Ϊ
��1��λ�ã�-CHO��2��λ�ã���-OH��2��λ�ã�-CHO��2��λ�ã���-OH��3��λ�ã�-CHO��3��λ�ã���7��ͬ���칹�壻����Ϊ![]() ������Hԭ�ӱ�OH��CHOȡ����OH��1��λ�ã���CHO��3��λ�����ʷ���������ͬ���칹�干��16�������к˴Ź���������4���,�ҷ����֮��Ϊ6:2:1:1����
������Hԭ�ӱ�OH��CHOȡ����OH��1��λ�ã���CHO��3��λ�����ʷ���������ͬ���칹�干��16�������к˴Ź���������4���,�ҷ����֮��Ϊ6:2:1:1����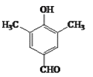 ��
�� ��
��
�ʴ�Ϊ��16��  ��
�� ��
��
��6������Ŀ�ģ�![]() ��
��![]() ��Ҫ��-CH3����Ϊ-COOH����Ҫ����λ����1��-NH2��������-CH3���������Ը�����������±�����Ϊ-COOH������֪��Ϣ��֪���������ڼױ�������-NO2��������������Ӧ��Ȼ����Fe/HCl�������½�-NO2��ԭΪ-NH2��������֪-NH2���ױ�����������-CH3������Ӧ��-NO2�Ļ�ԭ֮ǰ���ϳ�����ͼΪ��
��Ҫ��-CH3����Ϊ-COOH����Ҫ����λ����1��-NH2��������-CH3���������Ը�����������±�����Ϊ-COOH������֪��Ϣ��֪���������ڼױ�������-NO2��������������Ӧ��Ȼ����Fe/HCl�������½�-NO2��ԭΪ-NH2��������֪-NH2���ױ�����������-CH3������Ӧ��-NO2�Ļ�ԭ֮ǰ���ϳ�����ͼΪ�� ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ̽��SO2�Ļ�ѧ���ʣ����������ʵ��װ�á�
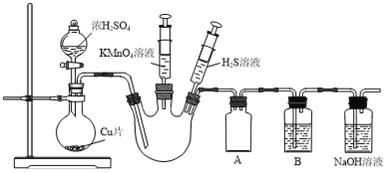
��1����װ������д��ڵ�������___________________��
��2��װ��A��������___________________��
��3���ٵ�������ƿ�г���SO2���壬֤��SO2���������Ե�ʵ�������������___________________��
����Ҫ֤��SO2����Ư���ԣ�����ϴ��ƿB�м���___________________��Һ��
��4��NaOH��Һ��������β���е�SO2�����ڿ�����������Һ�п��ܻ����SO![]() ��������Һ���Ƿ����SO
��������Һ���Ƿ����SO![]() ��ʵ�鷽����___________________��
��ʵ�鷽����___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ҩƷ�DZ�ˮ�����ϳ�·����ͼ���ش��������⣺ 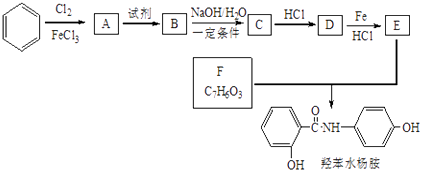
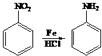
��֪�� 
��1���DZ�ˮ��ķ���ʽΪ �� �����DZ�ˮ�������˵����ȷ���ǣ�����ţ���
a.1mol�DZ�ˮ������Ժ�2mol NaOH��Ӧ
b�����ܷ���������Ӧ
c���ɷ���ˮ�ⷴӦ
d�������巢��ȡ����Ӧ
��2��D������Ϊ ��
��3��A��B�����Լ�Ϊ��D��E��Ӧ���л���Ӧ������ ��
��4��B��C��Ӧ�Ļ�ѧ����ʽΪ ��
��5��д�� F��ͬ���칹���м�����FeCl3������ɫ��Ӧ�����ܷ���������Ӧ�ģ������к˴Ź���������ʾ4��壬�ҷ����֮��Ϊ1��2��2��1��ͬ���칹���һ�ֽṹ��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������и�װ��ͼ������������ȷ����

A. ������װ�â�������������c��Ϊ������d��Ϊ�������������ҺΪAgNO3��Һ
B. װ�â���ԭ��أ��ܽ���ѧ��ת��Ϊ���ܣ�SO42������п�缫
C. װ�â���X��Ϊ���Ȼ�̼���������հ������Ȼ��⣬��������
D. װ�âܿ������ռ������������ն���İ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����ڱ���ǰ�����ڵ�����Ԫ��A��B��C��D��E��F�˵����������������Aԭ�Ӻ���������δ�ɶԵ��ӣ�������B2E�ľ���Ϊ���Ӿ��壬Eԭ�Ӻ����M���������ԳɶԵ��ӣ�CԪ���ǵ��к�����ߵĽ���Ԫ�أ�D���ʵ��۵���ͬ����Ԫ���γɵĵ���������ߵģ�F2�����Ӻ��������Ӿ������������������Ϣ���ش��������⣺
��1��A��B��C��D�ĵ�һ��������С�����˳��Ϊ______����Ԫ�ط��ű�ʾ��
��2��B���Ȼ�����۵��D���Ȼ�����۵�ߣ�������______��
��3��E�������������ӵĿռ乹����______����______���ӣ�����ԡ����Ǽ��ԡ���
��4��Fԭ�ӵļ۲�����Ų�ʽ��_____��
��5��E��F�γ�ij�ֻ���������ͼ��ʾ���־���ṹ����ɫ���ʾFԭ�ӣ����仯ѧʽΪ_____����a����Eԭ�ӵ���λ��Ϊ______�����ڣ�b���Ľṹ��ȡ��һ��ƽ����������Ϊ��������ƽ��һ�������к���_____��Fԭ�ӡ��ṹ��a���루b���о�����ԭ�ӿռ���������ȣ���a��________��b�����>����<����=����
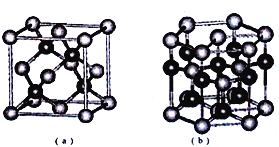
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������֢�����Ұ����������ڷ�������л�����������Ŵ�������ת���������£� 
����˵��������ǣ� ��
A.�Ұ�����������ᷴӦ������NaOH��Һ��Ӧ
B.���DZ���ͪ���������3�ֺ���������
C.1 mol����������뺬3 mol NaOH����Һ��Ӧ
D.������ˮ������DZ���ͪ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤����������ֵ������������ȷ����
A. 78g���к��е�̼̼˫������ĿΪ3NA
B. 16gCu2S��CuO��ɵĻ�����к��е���������Ϊ0.2NA
C. ��1mol H2�� 1 mol I2����һ�ܱ������г�ַ�Ӧ��ת�Ƶĵ�����Ϊ2NA
D. 1 mol Fe ��������Ũ���Ṳ�ȷ�Ӧ������SO2�ķ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�������ж���ȷ����
A. 0.1 mol Na2O2���е���������Ϊ0.4NA
B. ���³�ѹ�£�18g H2O ������������Ϊ8NA
C. 5.6 g�����������ᷴӦת�Ƶĵ�����Ϊ0.3NA
D. ����0.l mol FeCl3�ı�����Һ�Ƴɽ���������ɵ�Fe(OH)3������ĿΪ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ����2mol/L��NaCl��Һ980 ml������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ��NaCl�������ֱ����� ��
A. 980 mL��114.7g B. 500mL�� 58.5g
C. 1000 mL�� 117 g D. 1000mL��117.0g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com