
ЁОЬтФПЁПФГЛЏбЇаЫШЄаЁзщЮЊЬНОПSO2ЕФЛЏбЇаджЪЃЌЩшМЦСЫШчЯТЪЕбщзАжУЁЃ
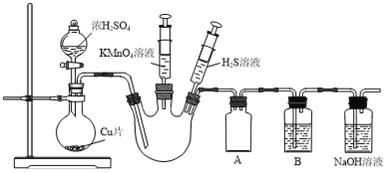
ЃЈ1ЃЉИУзАжУЩшМЦжаДцдкЕФЮЪЬтЪЧ___________________ЁЃ
ЃЈ2ЃЉзАжУAЕФзїгУЪЧ___________________ЁЃ
ЃЈ3ЃЉЂйЕБШ§ОБЩеЦПжаГфТњSO2ЦјЬхЃЌжЄУїSO2ОпгабѕЛЏадЕФЪЕбщВйзїМАЯжЯѓЪЧ___________________ЁЃ
ЂкШєвЊжЄУїSO2ОпгаЦЏАзадЃЌПЩдкЯДЦјЦПBжаМгШы___________________ШмвКЁЃ
ЃЈ4ЃЉNaOHШмвКгУгкЮќЪеЮВЦјжаЕФSO2ЃЌгЩгкПеЦјбѕЛЏЃЌШмвКжаПЩФмЛсДцдкSO![]() ЃЌМьбщШмвКжаЪЧЗёДцдкSO
ЃЌМьбщШмвКжаЪЧЗёДцдкSO![]() ЕФЪЕбщЗНЗЈЪЧ___________________ЁЃ
ЕФЪЕбщЗНЗЈЪЧ___________________ЁЃ
ЁОД№АИЁП CuКЭХЈH2SO4ЕФЗДгІШБЩйМгШШзАжУ ЗРжЙЕЙЮќ РЃЈЭЦЃЉЖЏзАгаH2SШмвКзЂЩфЦїЕФЛюШћЃЌзЂЩфЦїЃЈШ§ОБЩеЦПЃЉжаГіЯжЛызЧЯжЯѓ ЦЗКьШмвК ШЁЩйаэЮќЪеЮВЦјКѓЕФШмвКгкЪдЙмжаЃЌМгШызуСПЯЁбЮЫсЃЌдйМгШыBaCl2ШмвКЃЌШєГіЯжАзЩЋГСЕэЃЌдђЫЕУїДцдкSO![]() ЃЌШєЮоГСЕэЩњГЩЃЌдђВЛДцдкSO
ЃЌШєЮоГСЕэЩњГЩЃЌдђВЛДцдкSO![]()
ЁОНтЮіЁПЃЈ1ЃЉCuКЭХЈH2SO4ЕФЗДгІашвЊМгШШЃЌЖјИУзАжУЩшМЦжаШБЩйМгШШзАжУЁЃ
ЃЈ2ЃЉЦјЬхЗЂЩњзАжУЩњГЩЕФSO2ЦјЬхНјШыШ§ОБЩеЦПжаЃЌШєШ§ОБЩеЦПгвВрЕМЦјЙмжБНггыBзАжУЯрСЌЃЌдђШнвзВњЩњЕЙЮќЃЌЙЪAзАжУЕФзїгУЪЧЗРжЙЕЙЮќЁЃ
ЃЈ3ЃЉЂйгыШ§ОБЩеЦПСЌНгЕФЦфжавЛИізЂЩфЦїжаЪЂгаH2SШмвКЃЌЕБШ§ОБЩеЦПжаГфТњSO2ЦјЬхЃЌПЩРћгУSO2гыH2SЕФЗДгІжЄУїЦфОпгабѕЛЏадЃЌЪЕбщВйзїМАЯжЯѓЪЧЃКРЖЏзАгаH2SШмвКзЂЩфЦїЕФЛюШћЃЌзЂЩфЦїжаГіЯжЛызЧЯжЯѓЃЈЛђЭЦЖЏзАгаH2SШмвКзЂЩфЦїЕФЛюШћЃЌШ§ОБЩеЦПжаГіЯжЛызЧЯжЯѓЃЉЁЃЂкSO2ПЩвдЪЙЦЗКьШмвКЭЪЩЋЃЌБэЯжСЫЦфЦЏАзадЃЌЫљвдШєвЊжЄУїSO2ОпгаЦЏАзадЃЌПЩдкЯДЦјЦПBжаМгШыЦЗКьШмвКЁЃ
ЃЈ4ЃЉгЩвбжЊЃЌШмвКжаКЌгаSO32-ЃЌвЊМьбщЪЧЗёЛЙДцдкSO42-ЃЌашХХГ§ИЩШХЃЌЫљвдЪЕбщЗНЗЈЮЊЃКШЁЩйСПЮќЪеЮВЦјКѓЕФШмвКгкЪдЙмжаЃЌМгШызуСПЯЁбЮЫсЃЌдйМгШыBaCl2ШмвКЃЌШєГіЯжАзЩЋГСЕэЃЌдђЫЕУїДцдкSO42-ЃЌШєЮоГСЕэЩњГЩЃЌдђВЛДцдкSO42-ЁЃ


 ПкЫуаФЫуЫйЫугІгУЬтЯЕСаД№АИ
ПкЫуаФЫуЫйЫугІгУЬтЯЕСаД№АИ ЭЌВНЭиеЙдФЖСЯЕСаД№АИ
ЭЌВНЭиеЙдФЖСЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮяжЪЪєгкЭЌЯЕЮяЕФЪЧЃЈ ЃЉ
A.CH4гыCH3CH3
B.![]() гы
гы ![]()
C.CH3COOHгыC2H6O
D.CH3CH2CH2BrгыCH3CH2CH3
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдввЯЉЛљБНМзЫсЪЧживЊЕФвНвЉжаМфЬхЃЌЙуЗКгІгУгкКЯГЩИаЙтВФСЯЁЃЖдввЯЉЛљБНМзЫсПЩЭЈЙ§ШчЯТЗДгІКЯГЩЁЃ
ЗДгІЂйЃК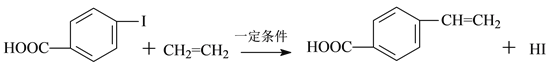
I II
ЃЈ1ЃЉЯТСаЙигкЛЏКЯЮяIКЭЛЏКЯЮяIIЕФЫЕЗЈЃЌе§ШЗЕФЪЧ______ЁЃ
A.ЛЏКЯЮяIФмгыаТжЦЕФCu(OH)2ЗДгІ
B.ОљПЩЗЂЩњѕЅЛЏЗДгІКЭвјОЕЗДгІ
C.ЛЏКЯЮяIIФмЪЙKMnO4ШмвКЭЪЩЋ
D.1molЛЏКЯЮяIIзюЖрФмгы5 mol H2ЗДгІ
ЃЈ2ЃЉЛЏКЯЮяIIЕФЗжзгЪНЮЊ____________ЃЌЛЏКЯЮяIIдкДпЛЏМСЬѕМўЯТЩњВњИпЗжзгЛЏКЯЮяЕФЗДгІЗНГЬЪН___________________________________________________________ЁЃ
ЃЈ3ЃЉЛЏКЯЮяIIПЩгЩЗМЯузхЛЏКЯЮяЂѓЭЈЙ§ЯћШЅЗДгІЛёЕУЃЌЂѓКЭCuЙВШШЕФВњЮяФмЗЂЩњвјОЕЗДгІ,аДГіЛЏКЯЮяЂѓЕФНсЙЙМђЪН_______________________ЃЛ
ЃЈ4ЃЉЛЏКЯЮяIVЪЧЛЏКЯЮяIIЕФЭЌЗжвьЙЙЬхЃЌЧвЛЏКЯЮяIVгіFeCl3ШмвКЯдзЯЩЋЃЌБНЛЗЩЯЕФвЛТШДњЮяжЛга2жжЃЌаДГіЛЏКЯЮяIVЕФНсЙЙМђЪН____________________________ЃЈаДвЛжжЃЉЁЃ
ЃЈ5ЃЉРћгУРрЫЦЗДгІЂйЕФЗНЗЈЃЌНівдфхБНЃЈ![]() ЃЉКЭШщЫсЃЈ
ЃЉКЭШщЫсЃЈ![]() ЃЉЮЊгаЛњЮядСЯКЯГЩЛЏЙЄдСЯШтЙ№ЫсЃЈ
ЃЉЮЊгаЛњЮядСЯКЯГЩЛЏЙЄдСЯШтЙ№ЫсЃЈ![]() ЃЉЃЌЩцМАЕФЗДгІЗНГЬЪНЮЊ________________________________ЃЛ___________________________________ЁЃ
ЃЉЃЌЩцМАЕФЗДгІЗНГЬЪНЮЊ________________________________ЃЛ___________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаЙиЮяжЪЕФзЊЛЏЙиЯЕШчЯТЭМЫљЪОЃЈВПЗжЮяжЪКЭЬѕМўвбТдШЅЃЉЁЃAЁЂBЁЂEЁЂGЁЂHЁЂJГЃЮТЯТЮЊЦјЬхЃЌAЮЊЛЦТЬЩЋЃЌJЮЊКьзиЩЋЃЌBФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЃЌEЪЧПеЦјжаКЌСПзюЖрЕФЦјЬхЃЌCЙЄвЕЩЯгУгкжЦШЁЦЏАзЗлЃЌKЮЊвЛжжКьЩЋН№ЪєЕЅжЪЃЌIЪЧГЃМћЕФЮоЩЋвКЬхЁЃ

ЃЈ1ЃЉEЕФЕчзгЪНЮЊ___________________ЁЃ
ЃЈ2ЃЉЗДгІЂкЕФЛЏбЇЗНГЬЪНЮЊ___________________ЁЃ
ЃЈ3ЃЉаДГіЗДгІЂлЕФЛЏбЇЗНГЬЪНЃЌВЂгУЕЅЯпЧХБэЪОЕчзгзЊвЦЕФЗНЯђКЭЪ§ФПЃК___________________ЁЃ
ЃЈ4ЃЉЗДгІЂнЕФРызгЗНГЬЪНЮЊ___________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЁА84ЁБЯћЖОвКЪЧвЛжжвдNaClOЮЊжїЕФЯћЖОМСЃЌЙуЗКгІгУгквНдКЁЂЪГЦЗМгЙЄЁЂМвЭЅЕШЕФЮРЩњЯћЖОЁЃ
ЃЈ1ЃЉЁА84ЁБЯћЖОвКжаЭЈШыCO2ФмдіЧПЯћЖОаЇЙћЃЌаДГіЯђЁА84ЁБЯћЖОвКжаЭЈШыЙ§СПCO2ЕФРызгЗНГЬЪНЃК___________________ЁЃ
ЃЈ2ЃЉВтЖЈЁА84ЁБЯћЖОвКжаNaClOЕФЮяжЪЕФСПХЈЖШЕФЗНЗЈШчЯТЃК
ЂйХфжЦ100.00mL 0.5000 molЁЄLЃ1ЕФNa2S2O3ШмвКЁЃХфжЦЙ§ГЬжаашзМШЗГЦШЁNa2S2O3ЙЬЬх___________________gЃЌашвЊгУЕНЕФВЃСЇвЧЦїгаЩеБЁЂНКЭЗЕЮЙмЁЂСПЭВЁЂ___________________ЁЃ
ЂкзМШЗСПШЁ10.00 mLЯћЖОвКгкзЖаЮЦПжаЃЌМгШыЙ§СПЕФKIШмвКЃЌгУзуСПЕФввЫсЫсЛЏЃЌГфЗжЗДгІКѓЯђШмвКжаЕЮМгNa2S2O3ШмвКЃЌЭъШЋЗДгІЪБЯћКФNa2S2O3ШмвК25.00 mLЁЃЗДгІЙ§ГЬжаЕФЯрЙиРызгЗНГЬЪНЮЊЃК
2CH3COOH+2IЁЊ+ClOЁЊ=I2+ClЁЊ+2CH3COOЁЊ+H2OЃЌI2+2S2O![]() =2IЁЊ+S4O
=2IЁЊ+S4O![]()
ЭЈЙ§МЦЫуЧѓГіИУЁА84ЁБЯћЖОвКжаNaClOЕФЮяжЪЕФСПХЈЖШЁЃЃЈаДГіМЦЫуЙ§ГЬЃЉ__________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮЂСЃжаЃЌжазгЪ§КЭжЪзгЪ§ЯрЕШЕФЪЧЃЈ ЃЉ
Ђй18OЃЛЂк12CЃЛЂл26MgЃЛЂм40KЃЛЂн40Ca
A.ЂйЂкB.ЂкЂнC.жЛгаЂмD.ЂлЂм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдгаЛњЮяЃК  ЕФЯТСаЫЕЗЈжаВЛе§ШЗЕФЪЧЃЈ ЃЉ
ЕФЯТСаЫЕЗЈжаВЛе§ШЗЕФЪЧЃЈ ЃЉ
A.ГЃЮТЯТФмгыNaHCO3ШмвКЗДгІЗХГіCO2
B.дкМюадЬѕМўЯТФмЗЂЩњЫЎНтЗДгІЃЌ1ФІИУгаЛњЮяЭъШЋЗДгІЯћКФЕє8ФІNaOH
C.гыЯЁH2SO4ЙВШШЃЌЩњГЩ2жжгаЛњЮя
D.ИУгаЛњЮяЕФЗжзгЪНЮЊC14H10O9
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌНЋФГвЛдЊЫсHAКЭNaOHШмвКЕШЬхЛ§ЛьКЯЃЌЪЕбщаХЯЂШчЯТЃК
ЪЕбщБрКХ | c(HA)molЁЄLЃ1 | c(NaOH)/molЁЄLЃ1 | ЗДгІКѓШмвКpH |
Мз | 0.1 | 0.1 | pH=9 |
вв |
| 0.2 | pH=7 |
ЯТСаХаЖЯВЛе§ШЗЕФЪЧЃЈ ЃЉ
A. 0.1![]() ЕФHAШмвКжагЩЫЎЕчРыГіЕФ
ЕФHAШмвКжагЩЫЎЕчРыГіЕФ![]()
B. ![]() вЛЖЈДѓгк0.2
вЛЖЈДѓгк0.2![]()
C. МзЗДгІКѓЕФШмвКжаЃКHAеМКЌAЮЂСЃзмЪ§ЕФ0.02ЃЅ
D. ввЗДгІЕФШмвКжаЃКc(NaЃЋ)Ѓ)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаЛњКЯГЩжЦвЉЙЄвЕжаЕФживЊЪжЖЮЁЃGЪЧФГПЙбзжЂвЉЮяЕФжаМфЬхЃЌЦфКЯГЩТЗЯпШчЯТЃК

вбжЊЃК
 ЃЈОпгаЛЙдадЃЌМЋвзБЛбѕЛЏЃЉЁЃ
ЃЈОпгаЛЙдадЃЌМЋвзБЛбѕЛЏЃЉЁЃ
ЃЈ1ЃЉBЕФНсЙЙМђЪНЮЊ ______ЁЃ
ЃЈ2ЃЉЗДгІЂмЕФЬѕМўЮЊ ___________ ЃЛЂйЕФЗДгІРраЭЮЊ ____________ ЃЛЗДгІЂкЕФзїгУЪЧ_________ ЁЃ
ЃЈ3ЃЉЯТСаЖдгаЛњЮяGЕФаджЪЭЦВте§ШЗЕФЪЧ __________ЃЈЬюбЁЯюзжФИЃЉЁЃ
AЃЎОпгаСНадЃЌМШФмгыЫсЗДгІвВФмгыМюЗДгІ
BЃЎФмЗЂЩњЯћШЅЗДгІЁЂШЁДњЗДгІКЭбѕЛЏЗДгІ
CЃЎФмОлКЯГЩИпЗжзгЛЏКЯЮя
DЃЎ1molGгызуСПNaHCO3ШмвКЗДгІЗХГі2molCO2
ЃЈ4ЃЉDгызуСПЕФNaHCO3ШмвКЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_______ЁЃ
ЃЈ5ЃЉЗћКЯЯТСаЬѕМўЕФCЕФЭЌЗжвьЙЙЬхга _____жжЁЃ
AЃЎЪєгкЗМЯузхЛЏКЯЮяЃЌЧвКЌгаСНИіМзЛљ
BЃЎФмЗЂЩњвјОЕЗДгІ
CЃЎгыFeCI3ШмвКЗЂЩњЯдЩЋЗДгІ
ЦфжаКЫДХЙВеёЧтЦзга4зщЗхЃЌЧвЗхУцЛ§жЎБШЮЊ6ЃК2ЃК2ЃК1ЕФЪЧ___ЃЈаДГіЦфжавЛжжНсЙЙМђЪНЃЉ
ЃЈ6ЃЉвбжЊЃКБНЛЗЩЯгаЭщЬўЛљЪБЃЌаТв§ШыЕФШЁДњЛљСЌдкБНЛЗЕФСкЖдЮЛЃЛБНЛЗЩЯгаЗхЛљЪБЃЌаТв§ШыЕФШЁДњЛљСЌдкБНвЛЦНЕФМфЮЛЁЃИљОнЬтжаЕФаХЯЂЃЌаДЯжвдМзБНЮЊдСЯКЯГЩгаЛњЮяЃЈ![]() ЃЉЕФСїГЬЭМЃЈЮоЛњЪдМСШЮбЁЃЉ________ЁЃКЯГЩТЗЯпСїГЬЭМЪОР§ШчЯТЃК
ЃЉЕФСїГЬЭМЃЈЮоЛњЪдМСШЮбЁЃЉ________ЁЃКЯГЩТЗЯпСїГЬЭМЪОР§ШчЯТЃК ![]() ФПБъВњЮяЁЃ
ФПБъВњЮяЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com