
【题目】下列表示化学反应A(g)+2B(g)=3C(g)+D(g)在不同条件下的反应速率,最快的是
A.υ(A)=0.3molL-1s-1B.υ(B)=0.5molL-1s-1
C.υ(C)=0.4molL-1s-1D.υ(D)=0.6molL-1s-1
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,已知A在标准状况下的密度为1.25g·L-1,D是塑料的主要成分,据此回答下列有关问题:

(1)A的结构简式为__________。
(2)反应⑤的反应类型为__________。
(3)反应⑥的方程式为__________。
(4)下列说法不正确的是__________。
A.通过石蜡油的裂化可以得到多种A的同系物,如丙烯
B.反应⑨的条件是氯气、光照
C.反应⑦的反应类型为消去反应
D.反应④为加聚反应,得到的产物可使酸性高锰酸钾溶液褪色
E.得到C有多种途径,通过途径⑧⑨得到C,产率较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绪(Ge)是半导体元素,应用广泛,回答下列问题:
(1)下列为Ge价电子层电子排布图表示的状态中,能量最低和最高的分别为____、_____(填选项)。
A.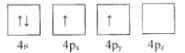 B.
B.
C.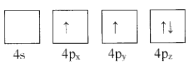 D.
D.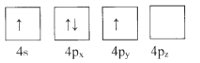
(2)GeH4的空间构型为____;比较与同锗族的氢化物的沸点如表所示,分析其变化规律及原因____。
CH4 | SiH4 | GeH4 | |
沸点/℃ | -161.5 | -119 | -88.1 |
(3)有机锗化合物A有一定的医疗保健作用,其结构简式为CF3N=GeH2,则Ge的杂化形式为____,碳原子与其它原子结合的键的种类为_____。
(4)Li2GeF6可以作为锂电池的电解质,则Li、Ge、F电负性由大到小的顺序为_____。
(5)Ge晶胞如下,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() ),D为(
),D为(![]() ,
,![]() ,
,![]() )。则C原子的坐标参数为_____。
)。则C原子的坐标参数为_____。
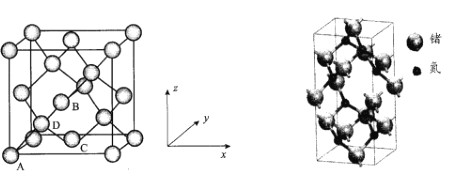
(6)氮化锗具有耐腐蚀、硬度高等优点,晶体中锗原子与氮原子之间存在明显的s-p杂化现象,氮化锗晶体属于____晶体。一种氮化锗晶胞的球棍模型如图,晶体中n(Ge)/n(N)=____,若晶胞底面正方形的边长为anm,阿伏加德罗常数值为NA,晶体的密度为ρg/cm3,则长方体的高为____nm(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯苯在染料、医药工业中用于制造苯酚、硝基氯苯、苯胺、硝基酚等有机中间体。实验室中制备氯苯的装置如图所示(夹持仪器已略去)。请回答下列问题:
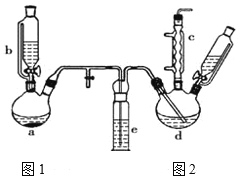
(1)仪器a中盛有KMnO4晶体,仪器b中盛有浓盐酸。打开仪器a中的活塞,使浓盐酸缓缓滴下,仪器中产生黄绿色气体,用离子方程式表示产生该现象的原因:____。
(2)仪器b中细玻璃导管的作用是_____。
(3)仪器d内盛有苯、FeCl3粉末,仪器a中生成的气体经过仪器e进入到仪器d中。
①仪器e的名称是洗气瓶,内盛装的试剂是____;
②仪器d中的反应进行过程中,保持温度在40-60℃,以减少副反应发生。仪器d的加热方式最好采用___加热。
(4)仪器c的作用是___;d中发生的化学反应方程式是____。
(5)该方法制备的氯苯中含有很多杂质,工业生产中通过水洗,然后通过碱洗,再水洗,最后通过分液得到含氯苯的有机物的混合物,混合物成分及沸点如图2表格所示:
有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
沸点/℃ | 80 | 132.2 | 180.4 | 173.0 | 174.1 |
①碱洗前先进行水洗的目的是____;
②取该有机物的混合物中的氯苯时,采用蒸馏的方法,收集___℃左右的馏分。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图,其中T原子的M层电子数比K层多2个,下列叙述不正确的是( )
![]()
A. 氢化物的稳定性:R<Q<T
B. T的单质是一种良好的半导体材料
C. Q、R的简单氢化物分子所含质子数、电子数与氖原子相同
D. T、W的最高价氧化物的水化物的酸性W强于T
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3,4―二羟基肉桂酸乙酯(I)具有抗炎作用和治疗自身免疫性疾病的潜力。由化合物A制备该物质的合成路线如图:
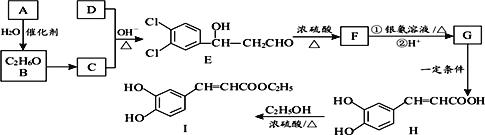
已知:R—CHO+R’—CH2—CHO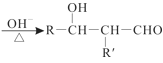
回答下列问题:
(1)A的结构简式为___,I中含氧官能团的名称是___。
(2)E生成F的反应类型为___。
(3)下列有关H的说法中,不正确的是___。
a.能使酸性高锰酸钾溶液褪色
b.1molH最多能和3molBr2反应
c.H分子中最多有9个碳原子共平面
d.1molH分别与足量NaOH、NaHCO3反应时,消耗的NaOH、NaHCO3的物质的量之比为1:1
(4)写出C+D→E的化学方程式___。
(5)已知W是H的同分异构体,符合下列条件的W结构共有___种。
①属于芳香族化合物。
②1molW与足量NaHCO3溶液反应生成气体44.8L(标准状况)。
其中,核磁共振氢谱有4组吸收峰,且峰面积比为1∶2∶2∶3的结构简式为:___(写一个即可)
(6)季戊四醇(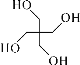 )是合成高效润滑剂、增塑剂、表面活性剂等的原料。设计由甲醛和乙醇为原料制备季戊四醇的合成路线(无机试剂任选)。合成路线的表示方法为:___。
)是合成高效润滑剂、增塑剂、表面活性剂等的原料。设计由甲醛和乙醇为原料制备季戊四醇的合成路线(无机试剂任选)。合成路线的表示方法为:___。
A![]() B……
B……![]() 目标产物。
目标产物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究H2O2分解的速率及影响因素,在相同温度下按照下表所示的方案完成实验。

(1)上述实验方案中,探究的变量因素只有催化剂的实验组合是_____和_____。
(2)实验④过程中氧气的生成速率和时间的趋势关系如图所示,判断该反应是反应(填“放热”或“吸热”)______。
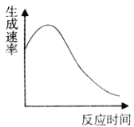
(3)实验⑤:在试管中加入10mL 0.4mol/L H2O2溶液,加入固体催化剂,在一定温度下测得不同时刻生成O2的体积(以折算为标准状况)如下表所示(假设反应过程溶液的体积保持不变):
![]()
①反应6min,H2O2分解了_______%。
②0至6min,以H2O2的浓度变化表示的反应速率为υ(H2O2)=________molL-1min-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液,所得滴定曲线如图所示(忽略混合时溶液体积的变化)。下列叙述不正确的是( )
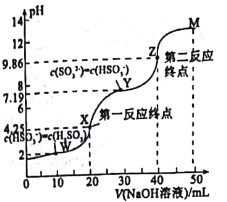
A.Ka2(H2SO3)的数量级为10-8
B.向X点加入少量澄清石灰水溶液,![]() 的值增大
的值增大
C.若将n(NaHSO3)与n(Na2SO3)=1:1混合,对应的点应在Y、Z之间
D.图中溶液中水的电离程度:W<X<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物与人类生产、生活密切相关。
(1)已知:S(s)+O2(g)= SO2(g) ΔH1=-a kJ·mol-1
S(g)+O2(g)= SO2(g) ΔH2=- b kJ·mol-1
则a___(填“>”或“<”)b。
(2)在一定温度和压强下,将2molSO2和1molO2置于密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g),并达到平衡。
2SO3(g),并达到平衡。
①若再加入1 molO2,该平衡向___(填“正”或“逆”)反应方向移动;
②若降低温度,达到平衡时测得SO2的含量减少,则正反应是___(填“吸热”或“放热”)反应;
③该反应的化学平衡常数表达式K=___。若只增大压强,则K__(填“增大”“减小”或“不变”)。
(3)常温下,现有0.5mol·L-1Na2SO3溶液,请判断:(Na2SO3第一步水解的离子方程式是SO32-+H2O![]() HSO3-+OH-)
HSO3-+OH-)
①该溶液的pH___(填“>”或“<”)7;
②该溶液中c(Na+)___(填“>”或“<”)2c(SO32-);
③盐类水解反应是吸热反应。加热该溶液,SO32-的浓度将__(填“增大”或“减小”)。
(4)如图是电解硫酸铜溶液的装置。
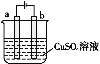
①若a、b为石墨电极,b电极的质量增加,写出该极的电极反应式:___;
②电镀是电解原理的一种重要应用。若利用该装置在铁件上镀铜,则铁件应与电源的__ (填“正极”或“负极”)连接。
(5)已知硫酸钡的沉淀溶解平衡为:BaSO4(s)![]() Ba2+(aq)+SO42-(aq) Ksp=1.0×10-10。在硫酸钡的饱和溶液中Ba2+的浓度为____mol·L-1。
Ba2+(aq)+SO42-(aq) Ksp=1.0×10-10。在硫酸钡的饱和溶液中Ba2+的浓度为____mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com