
25℃时,在等体积的①pH=0的H2SO4溶液、②0.05mol /L的Ba(OH)2溶液,③pH=5的NH4NO3溶液,④pH=10的Na2S溶液中,发生电离的水的物质的量之比是( )
/L的Ba(OH)2溶液,③pH=5的NH4NO3溶液,④pH=10的Na2S溶液中,发生电离的水的物质的量之比是( )
A.1:10:109:104 B.1:5:5×109:5×108 C.1:20:109:1010 D.1:10:109:1010
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源:2016-2017学年湖北省宜昌市高一上期中化学卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.氧化还原反应的本质是元素化合价的升降
B.氧化还原反应一定有氧元素参加
C.有单质参与的反应一定是氧化还原反应
D.发生氧化反应的物质也可能同时发生还原反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一上学期期中化学试卷(解析版) 题型:选择题
物质的量浓度相同的NaCl、MgCl2、AICl3兰种溶液,当它们的体积比为3:2:1时,三种溶液中Cl-的物质的量之比为( )
A. 3:4:3 B.1:1:1 C. 6:3:2 D. 1:2 :3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:选择题
已知水的电离平衡曲线如图所示,下列说法正确的是( )
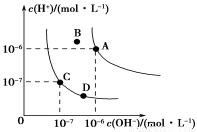
A.水的离子积常数 关系为:KW(B)>KW(A)>KW(C)>KW(D)
关系为:KW(B)>KW(A)>KW(C)>KW(D)
B.向水中加入醋酸钠固体,可以从C点到D点
C.B点对应的温度下,pH=4的硫酸与pH=10的氢氧化钠溶液等体积混 合,溶液的pH=7
合,溶液的pH=7
D.升高温度可实现由C点到D点
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:选择题
pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1 000 mL,其pH与溶液体积的关系如图19,下列说法正确的是( )
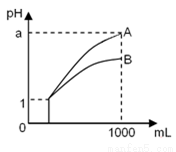
①若a<4,则A、B都是弱酸
②稀释后,A酸溶液的酸性比B酸溶液强
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:选择题
将0.1 mol·L-1醋酸溶液加水稀释,下列说法正确的是( )
A.溶液中c(OH-)和c(H+)都减小 B.溶液中c(H+)增大
C.醋酸电离平衡向左移动 D.溶液的pH增大
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三12月月考化学试卷(解析版) 题型:实验题
某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积百分数。
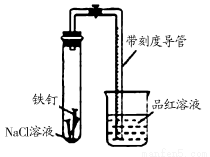
(1) 实验前用碱液清洗铁钉,再用0.100 mol/L的 H2SO4溶液浸泡至有气泡产生。用H2SO4溶液浸泡的目的是_________ _____。
(2) 为尽量减小误差,下列操作的正确顺序是 ___(填序号)。
①装入铁钉
②插入注射器向铁钉表面滴入适量NaCl溶液并打开止水夹
③将导管口浸入品红溶液
④塞上单孔活塞
⑤检查装置气密性
(3)实验中试管内发生的总反应化学方程式为 ;
用该实验方案测量空气中O2的体积百分数时应测量的数据是:
①导管与试管内部空间总体积,② _。
(4) 实验时发现上述测量过程因反应较慢耗时较长,对其影响因素作如下分析,请补充写出假设三:
假设一:电解质溶液的pH
假设二:NaCl溶液的浓度
假设三:________________
(5)借助上述实验装置,通过调节溶液的pH验证假设一,获得了如下实验数据:
pH | 2.0 | 5.5 | 6.0 | 6.5 | 7.0 | 8.0 |
液柱高度 | 0 cm | 1.3 cm | 8.5 cm | 8.4 cm | 8.5 cm | 8.5 cm |
形成稳定 液柱时间 | 3.0 min | 3.1 min | 5.1 min | 5.3 min | 15.6 min | min |
①当pH=2时,没有观察到稳定液柱形成的原因是_____________________。
②根据实验数据分析,为缩短实验测定时间,pH的最佳范围是________________。
③按上述实验装置,设计实验证明假设二。
第一步:配制不同浓度的NaCl溶液;
第二步:____________________,分别用注射器将NaCl溶液滴入铁钉表面;
第三步:记录形成稳定液柱所用时间和液柱的高度,比较分析数据得出结论。
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三12月月考化学试卷(解析版) 题型:填空题
(1)在配制氯化铁溶液时,为了防止发生水解,可以加入少量的 。
(2)氯化铝溶液具有净水的作用,原因是(用离子方程式表示): 。
(3)硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和水,常温下1g硅烷自燃放出的热量为a kJ,其热化学方程式为 。
(4)已知在密闭容器中将2.0molCO与10mol H2O混合加热到800℃,达到下列平衡:
CO (g) + H2O (g)  CO2 (g) + H2 (g) K=1.0则一氧化碳在此反应条件下的转化率是 。
CO2 (g) + H2 (g) K=1.0则一氧化碳在此反应条件下的转化率是 。
查看答案和解析>>
科目:高中化学 来源:2017届山东省德州市高三12月月考化学试卷(解析版) 题型:填空题
纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
①2Cu(s)+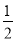 O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
②C(s)+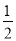 O2===CO(g) ΔH=-110.5 kJ·mol-1,
O2===CO(g) ΔH=-110.5 kJ·mol-1,
③2Cu(s)+ O2(g)===2CuO(s) ΔH=-314 kJ·mol-1
(1)则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为______________________。
(2)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
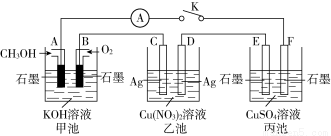
请回答下列问题:
①甲池为__________(填“原电池”“电解池”或 “电镀池”),A电极的电极反应式为______________
②丙池中电池总反应的离子方程式:_______________________
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为______mL(标准状况)。
④一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是________(填选项字母)。
A.CuO B. Cu C.Cu(OH)2 D.Cu2(OH)2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com