
物质的量浓度相同的NaCl、MgCl2、AICl3兰种溶液,当它们的体积比为3:2:1时,三种溶液中Cl-的物质的量之比为( )
A. 3:4:3 B.1:1:1 C. 6:3:2 D. 1:2 :3
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案科目:高中化学 来源:2016-2017学年江西省高二上学期期中化学试卷(解析版) 题型:选择题
浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随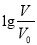 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( )
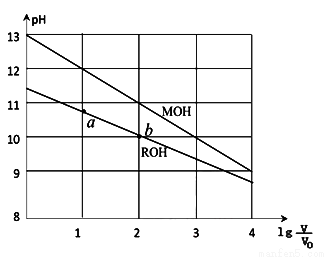
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当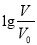 =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则  增大
增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高二上期中化学卷(解析版) 题型:填空题
(1)已知:①2Fe(s)+O2(g)=2 FeO(s)△H1=﹣544.0kJ•mol﹣1;
②4Al(s)+3O2(g)═2Al2O3(s)△H2=﹣3351.4kJ•mol﹣1。
Al和FeO发生铝热反应的热化学方程式是
(2)反应物与生成物均为气态的 某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
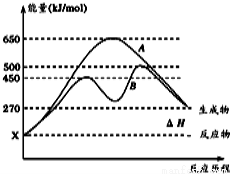
①据图判断该反应是 (填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,升高温度,逆反应速率将 (填“增大”、“减小”或“不变”)。
②其中B历程表明此反应采用的条件为 (填字母)。
A.升高温度 B.增大反应物的浓度
C.降低温度 D.使用催化剂
(3)已知热化学方程式:2H2(g)+O2(g)=2H2O(g)△H=﹣483.6kJ•mol﹣1,该反应的活化能为334.4kJ•mol﹣1,则其逆反应的活化能为  。
。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高二上期中化学卷(解析版) 题型:选择题
强酸和强碱稀溶液的中和热可表示为
H+(aq)+OH﹣(aq)=H2O(l) △H=﹣57.3kJ/mol
①HCl(aq)+NH3•H2O(aq)=NH4Cl(aq)+H2O(l) △H=﹣akJ/mol
②HCl(aq)+NaOH(s)=NaCl(aq)+H2O(l) △H=﹣bkJ/mol
③Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) △H=﹣ckJ/mol
则a,b,c三者的大小关系判断错误的是( )
A.c>114.6 B.a<57.3 C.b>57.3 D.2a=2b=c
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一上学期期中化学试卷(解析版) 题型:选择题
在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是( )
A.两种气体A与B的相对分子质量之比为m:n
B.同质量气体A与B的分子数之比为n:m
C.同温同压下,A、 B两气体的密度之比为n:m
D.相同状况下 ,同体积A、B两气体的质量之比为m:n
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一上学期期中化学试卷(解析版) 题型:选择题
某同学在研究新制饱和氯水成份的实验中,根据实验现象得出的结论不正确的是( )
A.氯水的颜色 呈浅黄绿色,说明氯
呈浅黄绿色,说明氯 水中含有Cl2
水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有CI-
C.向氯水中加入NaHCO 3粉末,有气泡产生,说明氯水中含有H+
3粉末,有气泡产生,说明氯水中含有H+
D.向淀粉碘化钾溶液中滴加少量氯水,溶液变蓝,说明氯水中含有ClO-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:实验题
在化学分析中,常需用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。实验室一般先称取一定质量的KMnO4晶体,粗配成大致浓度的KMnO4溶液,再用性质稳定、相对分子质量较大的基准物质草酸钠[ Na2C2O4 相对分子质量=134.0 ]对粗配的KMnO4溶液进行标定,测出所配制的KMnO4溶液的准确浓度,反应原理为: 5C2O42-+2MnO4-+16H+===10CO2↑+2Mn2++8H2O以下是标定KMnO4溶液的实验步骤:
步骤一:先粗配浓度约为0.15mol/L的KMnO4溶液500mL。
步骤二:准确称取Na2C2O4固体mg放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配KMnO4溶液进行滴定。记录相关数据。
步骤三: 。
步骤四:计算得KMnO4溶液的物质的量浓度。
试回答下列问题:
(1)下左图为整个过程中可能使用的仪器的部分结构(有的仪器被放大),
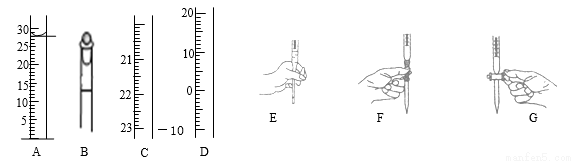
A图中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量某液体的体积,平视时读数为NmL,仰视时读数为MmL,若M>N,则所使用的仪器是 (填字母标号)。
(2)该滴定实验滴定终点的现象是 。
(3)步骤二中滴定操作图示(上右图)正确的是 (填编号)。
(4)步骤二的滴定过程温度变化并不明显,但操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色中间明显变快,最后又变慢的原因是 。
(5)请写出步骤三的操作内容 。
(6)若m的数值为1.340g,滴定的KMnO4溶液平均用量为25.00mL,则KMnO4溶液的浓度为 mol/L。
(7)若滴定完毕后读数时俯视,则实验误差为 (填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:选择题
25℃时,在等体积的①pH=0的H2SO4溶液、②0.05mol /L的Ba(OH)2溶液,③pH=5的NH4NO3溶液,④pH=10的Na2S溶液中,发生电离的水的物质的量之比是( )
/L的Ba(OH)2溶液,③pH=5的NH4NO3溶液,④pH=10的Na2S溶液中,发生电离的水的物质的量之比是( )
A.1:10:109:104 B.1:5:5×109:5×108 C.1:20:109:1010 D.1:10:109:1010
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三12月月考化学试卷(解析版) 题型:选择题
在一体积固定的密闭容器中,进行化学反应:2X(g) + Y(s) Z(g) + W(g);若其化学平衡常数(K)和温度(t)的关系如下表:
Z(g) + W(g);若其化学平衡常数(K)和温度(t)的关系如下表:
t/℃ | 700 | 800 | 900 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.3 | 1.8 | 2.7 |
对该反应而言,下列说法正确的是 ( )
A. 该反应正反应为放热反应
B.起始浓度不变,K越大,反应物的转化率越大
C.温度不变,增加X的用量,K增大
D.达平衡后,加入催化剂,K增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com