
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度。在H2SO4溶液中,反应如下:
2MnO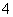 +5C2O
+5C2O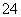 +16H+
+16H+ 2Mn2++10CO2↑+8H2O。
2Mn2++10CO2↑+8H2O。
(1)若用托盘天平称取W g Na2C2O4晶体,称量开始时和称量结束时的共同操作步骤是____________________。若需移动游码,应用__________拨动游码。
(2)若将W gNa2C2O4配成100 mL标准溶液,移取20.00 mL置于锥形瓶中,则酸性KMnO4溶液应装在__________(填“酸式”或“碱式”)滴定管中。
判断滴定达终点的现象是____________________。
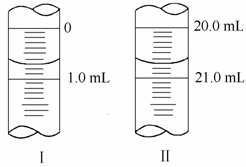
(3)若滴定管的起始读数和终点读数如图所示,则酸性KMnO4的物质的量浓度为____________________________(填表达式)。
(4)若滴定完毕立即读数,测定的KMnO4溶液的浓度__________(填“偏高”、“偏低”或“不变”)。
解析:(1)无论是添加砝码还是移动游码都不能用手去拿或拨动,而应用镊子,称量开始和结束都要进行的操作是把游码拨回零处。
(2)由于KMnO4具有强氧化性,可腐蚀乳胶管,故KMnO4应装入酸式滴定管中。当达到终点时,再滴入一滴KMnO4溶液,则溶液中因含有MnO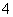 而呈紫色。
而呈紫色。
(3)由题图可知V(KMnO4)=20.70 mL-0.70 mL=20.00 mL,设KMnO4的物质的量浓度为x,
则:2MnO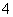 ~ 5C2O
~ 5C2O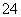
2 5
20.00×10-3 L·x 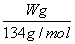 ×
×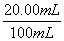
x=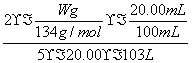 =
= mol/L。
mol/L。
(4)溶液变色因局部过量而实际未达终点,立即读数会造成V(KMnO4)减小,所以结果偏低。
答案:(1)把游码拨回零处 镊子
(2)酸式 滴入一滴酸性KMnO4溶液,溶液由无色变为紫色,且半分钟内不褪色
(3) mol/L (4)偏低
mol/L (4)偏低


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
在压强为2.20×104 kPa、温度达到374℃时,水成为“超临界状态”,此时水可将CO2等含碳化合物转化为有机物,这就是“水热反应”。生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源。下列说法不正确的是( )
A.二氧化碳与超临界水作用生成汽油的反应,属于放热反应
B.“水热反应”是一种复杂的化学变化
C.火力发电厂可望利用废热,将二氧化碳转变为能源物质
D.随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环
查看答案和解析>>
科目:高中化学 来源: 题型:
把4.6 g钠放入100 mL 0.1 moL/L AlCl3溶液中,待其充分反应后(溶液体积不变),下列叙述中错误的是( )。
A.Cl-浓度不变 B.溶液仍有浑浊
C.溶液中几乎不存在Al3+ D.溶液中存在最多的是Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
容积的相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g)+O2(g)2SO3(g),并达到平衡状态。在这个过程中,甲容器保持压强不变,乙容器保持容积不变。若甲容器中SO2的平衡转化率为P%,则乙容器中SO2的平衡转化率( )
A.等于P% B.大于P%
C.小于P% D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
在溶液中加入足量Na2O2后仍能大量共存的离子组是( )
A.NH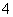 、Ba2+、Cl-、NO
、Ba2+、Cl-、NO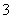
B.K+、AlO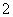 、Cl-、SO
、Cl-、SO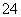
C.Ca2+、Mg2+、NO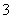 、HCO
、HCO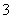
D.Na+、Cl-、CO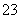 、SO
、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
如图拴上金属条的铁钉插在含有酚酞的NaCl溶液中,可以看到贴近金属条一边的溶液出现粉红色,该金属条可能是( )
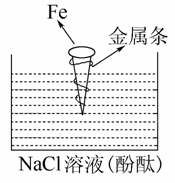
A.Cu B.Al
C.Zn D.Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:mX(g)+nY(g)qZ(g) ΔH<0,m+n>q,在恒容的密闭容器中反应达到平衡时,下列说法正确的是( )
A.通入稀有气体,压强增大,平衡正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.增加X的物质的量,Y的转化率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿佛加德常数,下列叙述中正确的是
A.分子数为NA的O2与CH3OH的混合物质量为32g
B. 0.1 mol/LNa2S溶液中所含S2-总数小于O.1NA
C. 1.5molNO2与足量H2O反应,转移的电子数为1mol
D. 32g铜与足量浓硫酸在加热条件下充分反应,生成11.2L气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com