
容积的相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g)+O2(g)2SO3(g),并达到平衡状态。在这个过程中,甲容器保持压强不变,乙容器保持容积不变。若甲容器中SO2的平衡转化率为P%,则乙容器中SO2的平衡转化率( )
A.等于P% B.大于P%
C.小于P% D.无法判断
科目:高中化学 来源: 题型:
已知25 ℃时,AgCl的溶度积Ksp=1.8×10-10,则下列说法正确的是
( )
A.向饱和AgCl水溶液中加入盐酸,Ksp变大
B.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-)
C.温度一定时,当溶液中c(Ag+)·c(Cl-)=Ksp时,此溶液中必有AgCl的沉淀析出
D.将AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,因为AgCl溶解度大于AgI
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应速率的说法正确的是( )
A.化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加
B.化学反应速率为0.8 mol·(L·s)-1是指1 s时某物质的浓度为0.8 mol·L-1
C.根据化学反应速率的大小可以知道化学反应进行的快慢
D.对于任何化学反应说,反应速率越大,反应现象就越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
将5.1 g镁铝合金溶于70 mL 4 mol/L硫酸中,当合金完全溶解后,再加入70 mL 8 mol/L的NaOH溶液,得沉淀的质量为13.6 g,则加入硫酸时,产生H2的物质的量为( )。
A.0.2 mol B.0.25 mol C.0.3 mol D.0.35 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L密闭容器中,盛有2 mol X和2 molY物质进行如下反应:2X(s)+3Y(g)Z(g),当反应进行10 s后,测得生成0.5 mol Z,则这期间的平均反应速率为( )
A.v(Z)=0.025 mol/(L·s)
B.v(X)=0.025 mol/(L·s)
C.v(Y)=0.05 mol/(L·s)
D.v(Y)=0.075 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
按照混合物、纯净物、强电解质、弱电解质、非电解质的顺序排列正确的一组是( )
A.盐酸、氯气、BaSO4、CO2、SO2
B.硫酸、氨水、醋酸、乙醇、NO2
C.漂白粉、胆矾、NH4Cl、CH3COOH、CO2
D.干冰、氯水、HCl、HClO、CO
查看答案和解析>>
科目:高中化学 来源: 题型:
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度。在H2SO4溶液中,反应如下:
2MnO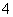 +5C2O
+5C2O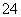 +16H+
+16H+ 2Mn2++10CO2↑+8H2O。
2Mn2++10CO2↑+8H2O。
(1)若用托盘天平称取W g Na2C2O4晶体,称量开始时和称量结束时的共同操作步骤是____________________。若需移动游码,应用__________拨动游码。
(2)若将W gNa2C2O4配成100 mL标准溶液,移取20.00 mL置于锥形瓶中,则酸性KMnO4溶液应装在__________(填“酸式”或“碱式”)滴定管中。
判断滴定达终点的现象是____________________。
(3)若滴定管的起始读数和终点读数如图所示,则酸性KMnO4的物质的量浓度为____________________________(填表达式)。
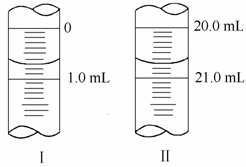
(4)若滴定完毕立即读数,测定的KMnO4溶液的浓度__________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同(0.2 mol/L)的弱酸HX与NaX溶液等体积混合后,溶液中微粒浓度关系错误的是( )
A.c(Na+)+c(H+)=c(X-)+c(OH-)
B.c(HX)+c(X-)=2c(Na+)
C.若混合液呈酸性,则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
D.若混合液呈碱性,则c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量m与加入Ba(OH)2的物质的量n之间的关系如图所示,下列说法正确的是
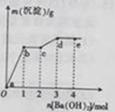
A. 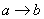 时的沉淀成分为BaSO4与Mg(OH)2
时的沉淀成分为BaSO4与Mg(OH)2
B. 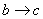 时发生的离子反应为H++OH-=H2O
时发生的离子反应为H++OH-=H2O
C. c点时的溶液中
D. 原混合溶液中:n(HCl)=2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com