
为了测定氢氧化钠固体混合物m g中碳酸钠的质量分数,某探究活动小组分别设计了如下实验方案:
(1)甲同学用如图一所示装置,通过测定放出CO2的体积来确定碳酸钠的质量分数,结果误差较大,请你提出改进措施 ;
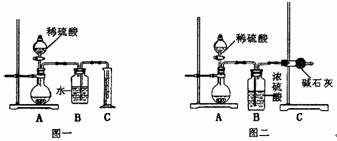
(2)乙同学用图二所示装置,通过测定反应放出CO2的质量来确定碳酸钠的质量分数,他重复正确操作三次,结果数据出现了较大偏差。你认为主要原因可能是(任写两个)
①
②
(3)丙同学认为上面的测定方法误差都较大,提出用中和滴定来测定。方法是:准确称取氢氧化钠样品m g,放入锥形瓶中加蒸馏水溶解,加1―2滴酚酞指示剂,用物质的量浓度为c mol?L―1的HCl溶液滴定至溶液由红色至无色(指示CO32―+H+=HCO3―反应的终点),消耗HCl溶液体积为V1mL,再加入1―2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙(指示H++HCO3―=CO2↑+H2O反应的终点),又消耗HCl溶液体积为V2ml。则烧碱样品中Na2CO3的质量分数为 ;
(4)请你设计另外一个简单的实验方案来测定NaOH固体混合物中Na2CO3的质量分数。
①写出操作步骤
②用测得的数据(用字母表示)写出质量分数的表达式 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
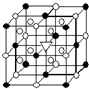 A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子
A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
| 80m-135n |
| 18n |
| 80m-135n |
| 18n |
查看答案和解析>>
科目:高中化学 来源:2008年江苏高考化学全真模拟二 题型:058
为了测定氢氧化钠固体混合物m g中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
(Ⅰ)甲同学的方案是:将样品溶解,加过量氯化钡溶液,过滤、洗涤、烘干,称量得固体n g.
(1)混合物中碳酸钠的质量分数为(用m、n表示)________.
(2)甲同学洗涤沉淀的操作是________________.
(3)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是:
①________________________;
②________________________;
(Ⅱ)乙同学的方案如图所示:
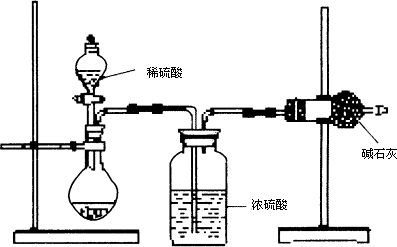
(1)根据乙同学的实验装置图分析,在每次实验中,完成测定过程至少要进行________次称量操作.
(2)他重复正确操作了三次,结果数据出现了较大的偏差,你认为主要原因可能是(任写三个):①________________________________;
②_______________________________________;
③_______________________________________.
查看答案和解析>>
科目:高中化学 来源:三点一测丛书 高中化学(选修)化学反应原理 江苏版课标本 江苏版课标本 题型:058
为了测定氢氧化钠和碳酸钠固体混合物m g中碳酸钠的质量分数,甲、乙、丙三位同学分别设计了如下的实验方案:
(1)甲同学的方案是:将样品溶解,加过量氯化钡溶液,过滤洗涤,取沉淀烘干,称量得固体n g.则混合物中碳酸钠的质量分数为________;若Ca2+、Ba2+都可使![]() 沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是________.
沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是________.
(2)乙同学的方案是:将样品溶解后,加入稍过量的氯化钡溶液,再滴入2~3滴________试液做指示剂,用标准盐酸滴定.乙同学在滴定过程中所需要的主要玻璃仪器有________、________.加入过量氯化钡溶液的目的是________.
(3)丙同学的方案如图所示:
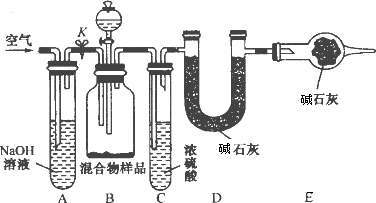
当混合物样品充分反应完全时,缓慢通入空气的目的是________,其中,装置A的作用是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)甲同学的方案是:将样品溶解,加入过量氯化钡溶液,过滤,将沉淀洗涤、烘干,称量所得固体质量为n g。
①检验沉淀已经洗净的方法为____________________________________________。
②此混合物中碳酸钠质量分数的计算式为_________________________________________。
(2)乙同学的方案是:将样品溶解,加入过量氯化钡溶液,再滴入2—3滴酚酞试液,用a mol/L标准盐酸滴定,到达滴定终点时消耗盐酸b mL。
①乙同学在滴定过程中所需要的主要玻璃仪器有______________、______________。
②此混合物中碳酸钠质量分数的计算式为______________。
(3)丙同学的方案如下图所示:
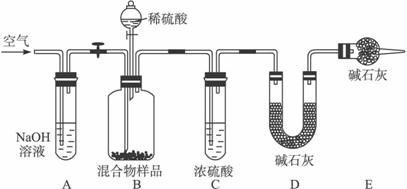
①装置C的作用是____________________________________________________。
②当混合物样品充分反应后,缓慢通入空气的目的是:_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com