
【题目】下列说法正确的是( )
A.2-苯基丙烯 ![]() 分子中所有碳原子一定在同一平面上
分子中所有碳原子一定在同一平面上
B.2-甲基-1,3-丁二烯与等物质的量的Br2发生加成反应,产物可能有3种。
C.在银镜反应中为快速析出银镜,我们一般采用玻璃棒搅拌加快反应速率
D.若苯中含有苯酚杂质,可加入浓溴水使苯酚生成三溴苯酚沉淀,然后过滤除去
科目:高中化学 来源: 题型:
【题目】“低碳”既是时尚,也是环保要求。“低碳”在工业生产中意义重大,充分利用原材料,不排放或减少排放“三废”,不同工厂今后联合生产等都是很好的“低碳”生产方式。下面是几个工厂利用废气、废渣(液)联合生产化肥硫酸铵的工艺:
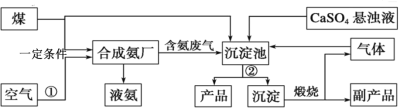
请回答下列问题:(提示:1、煤在一定条件下制取工业煤气,主要含H2、CO2等气体;2、操作①通常将空气液化后蒸馏分离出O2获得N2)
(1)工艺操作②为:_____。
(2)实验室用加热固体混合物的方法制备氨气的化学方程式为:_____。
(3)副产品的化学式为_____。该联合生产工艺中可以循环使用的物质是_____。
(4)在实验室中检验氨气的方法是_____。
(5)写出生成“产品”的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含Fe2+、I-、Br-的混合溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法正确的是( )

A.线段Ⅱ表示Br-的变化情况
B.原溶液中n(FeI2):n(FeBr2)=3:1
C.根据图像无法计算a的值
D.线段Ⅳ表示HIO3的变化情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B=H++HB-;HB-![]() H++B2-,回答下列问题:
H++B2-,回答下列问题:
(1)NaHB溶液显___(填“酸性”、“中性”或“碱性”或“无法确定”),理由是_______。
(2)某温度下,向0.1 mol·L-1 的NaHB溶液中滴入0.1 mol·L-1 KOH溶液至中性,此时溶液中以下关系一定正确的是________(填序号)。
a.c(H+)·c(OH-)=1×10-14 b.c(Na+)+c(K+)=c(HB-)+2c(B2-)
c.c(Na+)>c(K+) d.c(Na+)+c(K+)=0.05 mol·L-1
(3)已知0.1 mol·L-1NaHB溶液的pH=2,则0.1 mol·L-1H2B溶液中氢离子的物质的量浓度可能是________0.11 mol·L-1(填“<”、“>”或“=”); 理由是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计一个甲醚燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

根据要求回答相关问题:
(1)写出负极的电极反应式_____________________________。
(2)铁电极为________(填“阳极”或“阴极”),石墨电极(C)的电极反应式为________________。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将____(填“增大”、“ 减小”或“不变”)。
(4)若在标准状况下,有2.24L氧气参加反应,则丙装置中阴极析出铜的质量为______。假设乙装置中氯化钠溶液足够多,若在标准状况下,有224mL氧气参加反应,则乙装置中阳离子交换膜左侧溶液质量将____________(填“增大”、“减小”或“不变”),且变化了_______克。
(5)若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源、环保等方面有着广泛的用途。利用湿法、干法制备高铁酸盐的原理如表所示。
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
干法 | Fe2O3、KNO3、KOH混合加热生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上利用湿法制备高铁酸钾(K2FeO4)的流程如图所示:
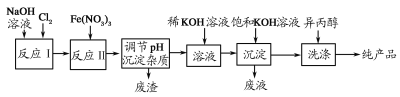
①反应Ⅰ的化学方程式为_____________。
②反应Ⅱ的离子方程式为_______________。
③加入饱和KOH溶液的目的_____________。
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为___________。
(3)干法制备K2FeO4的反应中,氧化剂是________。
(4)高铁电池是正在研制中的可充电干电池,如图为该电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有________、________。
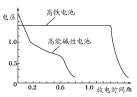
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅的冶炼过程大致如下:![]() 富集:将方铅矿
富集:将方铅矿![]() 进行浮选;
进行浮选;![]() 焙烧:
焙烧:![]()
![]()
![]() ;
;![]() 制粗铅:
制粗铅:![]()
![]()
![]() ,
,![]()
![]()
![]() 。下列说法正确的是:
。下列说法正确的是:
A.浮选法富集方铅矿的过程发生化学变化
B.将![]() 冶炼成Pb理论上至少需要
冶炼成Pb理论上至少需要![]()
C.整个冶炼过程中,制取![]() 共转移
共转移![]() 电子
电子
D.方铅矿焙烧的反应中,PbS是还原剂,还原产物只有PbO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向葡萄酒中加入Na2S2O5抗氧化。测定某葡萄酒中Na2S2O5残留量的方法:取50.00ml葡萄酒样品,用0.0100molL-1的碘标准液滴定至终点,消耗标准液10.00ml。则该样品中Na2S2O5的残留量为![]() 已知
已知![]()
![]()
A.0.001gL-1B.0.002gL-1C.0.064gL-1D.0.19gL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.电离平衡常数可以表示弱电解质的相对强弱
B.电离平衡常数受溶液浓度的影响
C.H2CO3的电离常数表达式:K=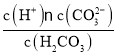
D.电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com