
【题目】下列说法正确的是( )
A.电离平衡常数可以表示弱电解质的相对强弱
B.电离平衡常数受溶液浓度的影响
C.H2CO3的电离常数表达式:K=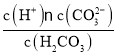
D.电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.2-苯基丙烯 ![]() 分子中所有碳原子一定在同一平面上
分子中所有碳原子一定在同一平面上
B.2-甲基-1,3-丁二烯与等物质的量的Br2发生加成反应,产物可能有3种。
C.在银镜反应中为快速析出银镜,我们一般采用玻璃棒搅拌加快反应速率
D.若苯中含有苯酚杂质,可加入浓溴水使苯酚生成三溴苯酚沉淀,然后过滤除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A常用于食品行业,已知9.2 g A在足量的O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,二者分别增重3.6g和8.8 g,经检验剩余气体为O2。
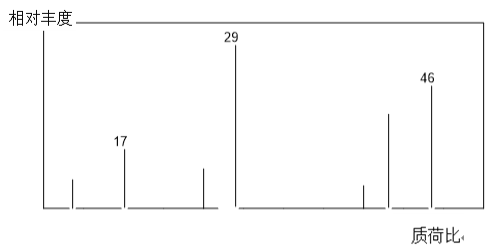
(1)有机物A的质谱图如下图所示,从图中可知其相对分子质量是___。
(2)A的结构简式为___。
(3)用A进行下列反应
①银镜反应:A在进行银镜反应之前必须在其中加入一定量的_______,因为_______。
②A发生银镜反应的化学方程式为_____________。
③写出A和乙醇反应的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单质硫在NaOH的热浓溶液中发生歧化反应,将2.56g硫与含0.0600molNaOH的热溶液反应恰好生成amolNa2Sx和bmolNa2S2O3,再加入1.00mol/L的NaClO溶液VmL,使溶液中所有硫元素全部转化为Na2SO4。计算:(1)a/b=________;
(2)V至少为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可由天然气为原料制备甲醇,也可由水煤气合成甲醇.
![]() 已知:
已知:![]() ,
,![]() ,
,![]() 。试写出由
。试写出由![]() 和
和![]() 制取甲醇的热化学方程式:______;
制取甲醇的热化学方程式:______;
![]() 通过下列反应制备甲醇:
通过下列反应制备甲醇:![]() ,图甲是反应时
,图甲是反应时![]() 和
和![]() 的浓度随时间t的变化情况,从反应开始到平衡,用
的浓度随时间t的变化情况,从反应开始到平衡,用![]() 表示平均反应速率
表示平均反应速率![]() ______,平衡时CO的转化______.
______,平衡时CO的转化______.
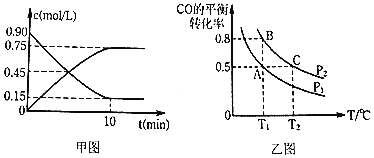
![]() 在一容积可变的密闭容器中充入
在一容积可变的密闭容器中充入![]() 和
和![]() ,CO的平衡转化率随温度
,CO的平衡转化率随温度![]() 、压强
、压强![]() 的变化如图乙所示.
的变化如图乙所示.
![]() 下列说法不能判断该反应达到化学平衡状态的是______
下列说法不能判断该反应达到化学平衡状态的是______![]() 填字母
填字母![]()
A ![]() 的消耗速率等于
的消耗速率等于![]() 的生成速率的2倍
的生成速率的2倍
B ![]() 的体积分数不再改变
的体积分数不再改变
C 体系中![]() 的转化率和CO的转化率相等
的转化率和CO的转化率相等
D 体系中气体的平均摩尔质量不再改变
![]() 比较A、B两点压强大小
比较A、B两点压强大小![]() ______
______![]() 填“
填“![]() 、
、![]() 、
、![]() ”
”![]()
![]() 若达到化学平衡状态A时,容器的体积为20L,如果反应开始时仍充入
若达到化学平衡状态A时,容器的体积为20L,如果反应开始时仍充入![]() 和
和![]() 2,则在平衡状态B时,容器的体积
2,则在平衡状态B时,容器的体积![]() ______L;
______L;
![]() 以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池
以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池![]() 电极材料为惰性电极
电极材料为惰性电极![]()
![]() 若KOH溶液足量,则电池负极反应的离子方程式为______;
若KOH溶液足量,则电池负极反应的离子方程式为______;
![]() 若电解质溶液中KOH的物质的量为
若电解质溶液中KOH的物质的量为![]() ,当有
,当有![]() 甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是______.
甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钙(Ca3N2)是一种重要的化学试剂,通常条件下为棕色易水解的固体。某小组在实验室制备氮化钙并测定其纯度,设计如下实脸(夹持装置略去):
I.氮化钙的制备。
(1)加热条件下,钙和氮气制备氮化钙的反应方程式为_________。

(2)按气流由左到右的方向,上述装置合理的连接顺字为__________(填仪器接口字母)。
(3)按连接好的装置进行实验。
①实验步骤如下,检查装置气密性,加入药品:_______(请按正确顺序填入下列步骤的字母标号)。
a.点燃装置C处酒精灯,反应一段时间
b.打开分液漏斗活塞
c.点燃装置A处酒精灯
d.熄灭装置A处酒精灯
e.熄灭装置C处酒精灯
f.关闭分液漏斗活塞
②装置B的作用为_________。
③装置C的硬质玻璃管中的现象为_________。
(4)设计实验证明Ca3N2中混有钙单质:_______________。
II.测定氮化钙纯度。
i.称取4.0g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1 .00mol/L盐酸中,充分反应后,将所得溶液稀释到200 . 00 mL;
ii.取20 . 00mL稀释后的溶液,用0 . 2mol/LNaOH标准溶液滴定过量的盐酸,到终点时消耗标准溶液25 . 00 mL。
(5)所取固体中氮化钙的质量分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示。据图判断正确的是 ( )
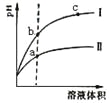
A.Ⅱ为盐酸稀释时pH变化曲线
B.a点Kw的数值比c点Kw的数值大
C.b点溶液的导电性比c点溶液的导电性强
D.b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期T、X、Y、Z、W、M六种元素,已知W、Z、X、T、Y五种非金属元素原子半径依次减小,其中W原子的s电子总数等于p电子总数的2倍,M原子的M能层上有4个未成对电子。请回答下列问题:
(1)写出W、Z、X、T四种元素第一电离能由大到小的顺序:____________(用元素符号表示)。
(2)基态M原子的核外电子排布式为__________________________。
(3)根据VSEPR理论,推断出由W与X两元素组成的最简单二价阴离子的立体构型为____________,W原子的杂化类型为____________。
(4)Y与T、X、Z、W所形成的最简单化合物的沸点由高到低的顺序为__________________________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗是第四周期第ⅣA族元素,锗是重要的半导体材料,用于制造晶体管及各种电子装置。下图为以锗锌矿(含GeO2、ZnS及少量Fe2O3)为原料生产高纯度锗的工艺流程如下:

已知:GeO2可溶于强碱溶液,生成锗酸盐。GeCl4的熔点为-49.5℃,沸点为84℃,在水中或酸的稀溶液中易水解。
回答下列问题:
(1)步骤①中提高碱浸效率的措施有______________________(写一种),NaOH溶液碱浸时发生反应的离子方程式为______________________。
(2)操作a的名称是___________,GeCl4的电子式为_______________。
(3)滤渣1中除含有ZnS外,还含有少量___________。滤渣2中除含有 CaGeO3外,还含有少量___________。
(4)步骤⑤中加入浓盐酸,发生反应的化学方程式为______________________。不用稀盐酸的原因是______________________。
(5)写出一种证明步骤⑧反应完全的操作方法:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com