
【题目】莽草酸的一种异构体A在浓硫酸作用下加热可得到B.下列说法不正确的是( )

A. X的化学式为H20
B. A既能使![]() 溶液褪色,又能使酸性
溶液褪色,又能使酸性![]() 溶液褪色
溶液褪色
C. B所有碳原子在同一平面上
D. 与B分子式相同,有三个官能团且苯环上的一氯取代物有两种的异构体只有一种
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3)是一种重要的化工原料。实验室制备BCl3的原理B2O3+3C+3Cl2 =2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。已知:BCl3的熔点为-107.3℃,沸点为12.5℃,遇水水解生成H3BO3和HCl,请回答下列问题:
(实验Ⅰ)制备BCl3并验证产物CO

(1)该实验装置中合理的连接顺序为G→_____→_____→_____→____→F→D→I。其中装置E的作用是___________________________。
(2)装置J中反应的化学方程式为____________________________________。
(实验Ⅱ)产品中氯含量的测定
①准确称取少许m克产品,置于蒸馏水中完全水解,并配成100mL溶液。
②取10.00mL溶液于锥形瓶中
③加入V1mL浓度为C1 mol/LAgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。
④以硝酸铁为指示剂,用C2 mol/L KSCN标准溶液滴定过量的AgNO3溶液。发生反应:Ag+ +SCN- =AgSCN↓。
⑤重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2 mL。
已知: Ksp(AgCl)>Ksp(AgSCN) 。
(3)步骤④中达到滴定终点的现象为__________________。
(4)实验过程中加入硝基苯的目的是___________________。
(5)产品中氯元素的质量分数为_________________%。
(6)下列操作,可能引起测得产品中氯含量偏高是__________。
A.步骤③中未加硝基苯
B.步骤①中配制100mL溶液时,定容时俯视刻度线
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气与适量氯气混合反应可生成NH4Cl(俗称脑砂)和一种无污染的气体。某学习小组利用下列装置模拟该反应,请回答相关问题。

(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为____;X中发生反应的离子方程式为_______。
(2)要得到干燥纯净的氯气,上述A、B、C装置的连接顺序依次为a→_____(用小写字母表示)。
(3)利用E装置,将适量氨气与氯气充分混合反应氨气应从_______(用小写字母表示)通入,反应的化学方程式为_______________;可能观察到的现象是___________。
(4)《唐本草》记载脑砂入药可以散瘀消肿,天然脑砂含少量NH4Cl,现取天然脑砂进行NH4Cl含量测定。准确称取一定质量脑砂,与足量的氧化铜混合,如下图所示进行实验。已知:2NH4Cl+3CuO=3Cu+N2+2HCl+3H2O 。
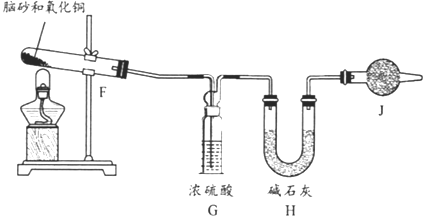
①为顺利完成有关物理量的测定,请完善下列表格:
测量时间点 | 加热前 | 当观察到_____现象时 |
测量内容 | _______________ | 停止加热,冷却,称量H装置的总质量 |
②如果不用J装置,测出NH4Cl的含量将_____(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期(即原子序数为1~18号)元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层上的电子数等于其内层电子数的差值 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下其单质为双原子分子,且占空气中的含量最大 |
Z | 该元素的某种含氧酸具有漂白性 |
(1)按要求用有关的化学用语填充:
T元素的离子符号:______;Y离子的电子式__________;Z离子的结构示意图_______________;
(2)元素Y与氢元素能形成一种10电子的阳离子,该微粒符号是____________;
(3)写出元素T的最高价含氧酸与X的最高价含氧酸对应的钠盐反应的化学方程式____
(4)元素Z与某一活泼金属元素组成的盐是重要的化工原料,写出其作为该原料在化工生产上电解的一个重要反应:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.煤的气化、煤的液化都是物理变化
B.石油是由多种烃组成的混合物
C.汽油都不能使溴水褪色
D.乙烷的产量可以衡量一个国家石油化工的发展水平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种从含Br-废水中提取Br2的过程,包括过滤、氧化、正十二烷萃取及蒸馏等步骤。已知:
Br2 | CCl4 | 正十二烷 | |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |

下列说法正确的是( )
A. 用甲装置过滤时,需不断搅拌
B. 用乙装置将Br-氧化为Br2
C. 丙装置中用正十二烷而不用CCl4,是因为其密度小
D. 可用装置丁进行蒸馏,先收集正十二烷再收集Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50mLNa2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,并有气体产生。
(1)原混合溶液中Na2SO4和Na2CO3的物质的量浓度各是______。
(2)产生的气体在标准状况下的体积是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77 | 137 | 遇水生成HCl、SO2、S;与过量氯气发生S2Cl2+Cl2 温度超300℃以上完全分解为硫和氯气 |
设计实验装置图如下:

(1)上图中气体发生和尾气处理装置不够完善,请你提出改进意见_______________________。
利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式为_________________________________________________________。
(3)C、D中的试剂分别是_________________、_____________________。
(4)仪器A、B的名称分别是___________、___________,F的作用是_______________________。
(5)如果在加热E时温度过高,对实验结果的影响_________________________________;在F中可能出现的现象是________________________________________________。
(6)S2Cl2粗品中可能混有的杂质是(填写两种物质的化学式)______________、_____________,为了提高S2Cl2的纯度,关键的操作是控制好温度和_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某盐酸的密度为![]() ,HCl的质量分数为
,HCl的质量分数为![]() ,试计算:
,试计算:
(1)该盐酸的物质的量浓度是多少?(小数点后保留两位)_________
(2)在足量的该盐酸溶液中,加入镁粉和铝粉混合物![]() ,充分反应共生成
,充分反应共生成![]() 气体(标准状况),求混合物中镁和铝的质量各为多少?____________,_______________
气体(标准状况),求混合物中镁和铝的质量各为多少?____________,_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com