
【题目】将过量的二氧化碳分别通入:①氯化钙溶液 ②硅酸钠溶液 ③氢氧化钙溶液 ④饱和碳酸钠溶液。最终溶液中有白色沉淀析出的是( )
A.①②③④
B.②④
C.①②③
D.②③
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列与金属腐蚀有关的说法正确的是( )
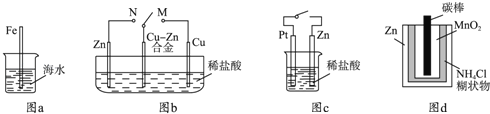
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu﹣Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn﹣MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由铝和某些金属氧化物组成的混合物在化学上称为铝热剂,该混合物在高温条件下能发生置换反应。为确定某铝热剂样品(铝和氧化铁)的组成,分别进行下列实验:
(1)若取10.7g该样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为aL。反应的化学方程式是__,样品中铝的质量分数是__(用含a的表达式表示)。
(2)若取同质量的样品,在高温下使其恰好反应,则a=__L;该反应的化学方程式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.05mol某有机物A和0.125molO2在一密闭容器中充分燃烧,所得产物通过浓H2SO4时使其增重2.7g;再通过足量灼热的CuO粉末,固体质量减小了0.8g;最后通过足量碱石灰,固体质量增加了6.6g。
(1)该化合物A的分子式______________。(写出计算过程)
(2)若0.05mol含有醛基的有机物B与有机物A的最简式相同,且在0.125molO2中能完全燃烧,写出B所有可能的结构简式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,CH3COOH溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,下列说法正确的是( )
CH3COO-+H+,下列说法正确的是( )
A. 向10mLpH=5的CH3COOH溶液中加水至10L,最后溶液pH在7和8之间
B. 加入少量CH3COONa固体,平衡向左移动,c(CH3COO-)下降
C. 加入少量NaOH固体(忽略溶解热效应),平衡向右移动,水的电离程度也随之增大
D. 向10mLpH=5的CH3COOH溶液中加入等体积,等浓度的盐酸,混合溶液的c(H+)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)偏铝酸钠溶液中逐滴加入盐酸至过量,可观察到的现象是____________________,反应的离子方程式是____________________________、____________________________。
(2)偏铝酸钠溶液中持续不断地通入二氧化碳,可观察到的现象是________________,反应的离子方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.根据类推思想,氯化铝溶液蒸干后灼烧,最后得到氧化铝,则硫酸铝也一样
B.高温高压下的超临界水,溶液中的氢离子和氢氧根离子浓度较大,有时显酸性,有时显碱性
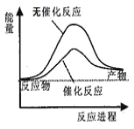
C.如图可表示水分解过程中的能量变化
D.等体积、等浓度的醋酸钠溶液和次氯酸钠溶液中,所含离子总数前者小于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气放出,下列叙述不正确的是( )
A.NH4H是离子化合物,含有离子键和共价键
B.NH4H与水反应时,NH4H是还原剂
C.NH4H投入少量的水中,有两种气体产生
D.NH4H溶于水,所形成的溶液成酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2二溴乙烷的反应原理如下:CH3CH2OH![]() CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
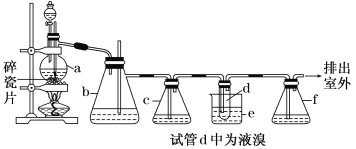
有关数据列表如下:
乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在装置c中应加入________(选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是______________________。
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的________(填“上”或“下”)层。
(4)若产物中有少量未反应的Br2,最好用________(填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是______________________; 但不用冰水进行过度冷却,原因_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com