
【题目】回答下列问题:
(1)偏铝酸钠溶液中逐滴加入盐酸至过量,可观察到的现象是____________________,反应的离子方程式是____________________________、____________________________。
(2)偏铝酸钠溶液中持续不断地通入二氧化碳,可观察到的现象是________________,反应的离子方程式是________________________。
【答案】开始产生白色沉淀,并不断增多;盐酸过量时沉淀溶解,最后完全消失 ![]() +H++H2O===Al(OH)3↓ Al(OH)3+3H+===Al3++3H2O 产生白色沉淀,并不断增多
+H++H2O===Al(OH)3↓ Al(OH)3+3H+===Al3++3H2O 产生白色沉淀,并不断增多 ![]() +CO2+2H2O===Al(OH)3↓+
+CO2+2H2O===Al(OH)3↓+![]()
【解析】
偏铝酸钠和过量的盐酸反应开始生成氢氧化铝沉淀,后氢氧化铝沉淀溶解,最后生成氯化铝和氯化钠,偏铝酸钠和过量的二氧化碳反应生成氢氧化铝沉淀,据此分析离子方程式。
(1)偏铝酸钠溶液中加入过量的盐酸,开始反应生成氢氧化铝沉淀和氯化钠,随着盐酸加入量的增加,氢氧化铝不断增多,最后又溶解为氯化铝,直到最后消失,离子方程式为 ![]() +H++H2O=Al(OH)3↓;Al(OH)3+3H+=Al3++3H2O;
+H++H2O=Al(OH)3↓;Al(OH)3+3H+=Al3++3H2O;
(2)偏铝酸钠和过量的二氧化碳反应开始生成氢氧化铝沉淀和碳酸钠,当二氧化碳过量时碳酸钠继续反应生成碳酸氢钠,现象为:产生白色沉淀,并不断增多,离子方程式为:![]() +CO2+2H2O=Al(OH)3↓+
+CO2+2H2O=Al(OH)3↓+![]() 。
。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,向1 L pH=10的 NaOH溶液中持续通入CO2。通入的CO2的体积(V)与溶液中水电离出的OH- 离子浓度(φ)的关系如下图所示。下列叙述不正确的是( )

A. a点溶液中:水电离出的c( H+ )=1×10-10mol/L
B. b点溶液中:c( H+ )=c( OH- )
C. c点溶液中:c(OH-) > c(HCO3-)+c( H+ )
D. d点溶液中:c(Na+)=2c(CO32-)+c(HCO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列六种物质的溶液:①NaCl ②NH4Cl ③Na2CO3 ④Al2(SO4)3 ⑤CH3COOH ⑥NaHCO3
(1)25℃时,0.1mol·L-1①溶液呈______性,0.1mol·L-1②溶液的pH________7(填“>”、“=”或“<”);其原因是______________________________________(用离子方程式表示);
(2)常温(填“>”、“=”或“<”)下,浓度均为0.1mol/L的③和⑥的溶液中离子种类________(填“相同”或是“不相同”),溶液的pH:③_________⑥(填“>”、“=”或“<”);
(3)将④溶液加热蒸干并灼烧最终得到的物质是____________(填化学式);
(4)常温下0.1 mol/L的⑤溶液加水稀释过程中,下列表达式的数据一定变大的是_________。
A.c(H+) B.  C.c(H+)·c(OH-)
C.c(H+)·c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下二氯化二硫(S2 Cl2)为红棕色液体,其结构式为Cl-S-S-Cl。其制备反应及与水反应的化学方程式如下:①CS2+3Cl2 ![]() CCl4+S2Cl2 ②2S2Cl2 +2H2O=4HCl+SO2↑+3S↓则下列说法正确的是 ( )
CCl4+S2Cl2 ②2S2Cl2 +2H2O=4HCl+SO2↑+3S↓则下列说法正确的是 ( )
A. 反应①中CS2作氧化剂
B. 反应②中S2Cl2既作氧化剂又作还原剂
C. 反应①中每生成1mol S2Cl2转移4mol电子
D. 反应②中氧化产物与还原产物的物质的量之比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 氢化钙固体登山运动员常用的能源提供剂.某兴趣小组长拟选用如下装置制备氢化钙.
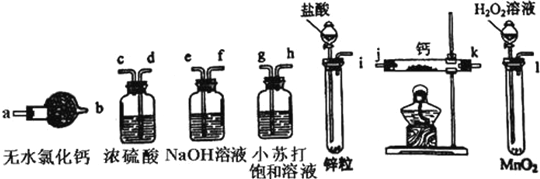
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为__________(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞_________(请按正确的顺序填入下列步骤的标号).
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭分液漏斗活塞 D.停止加热,充分冷却
(3)已知钙与氢化钙固体在外观上相似,现设计一个实验,用化学方法区分钙与氢化钙,请完善以下实验的简要步骤及观察到的现象:取适量氢化钙,在加热条件下与 _________反应,将反应气相产物通过装有_______的容器,观察到容器内固体颜色变化为__________;取钙做类似实验,观察不到类似的反应现象.
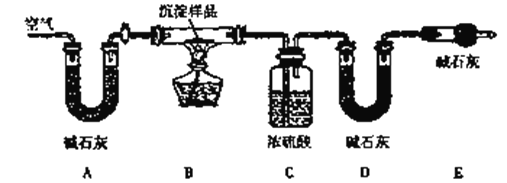
II.某化学兴趣小组发现,往CuSO4溶液中加入一定浓度的Na2CO3溶液得到的蓝色沉淀,若加入NaOH溶液则得到浅绿色沉淀。为此,小组同学对蓝色沉淀成份作了如下探究:
该小组同学利用下列装置通过实验测定其组成
(1)检查装置气密性并装好药品后,点燃酒精灯前应进行的操作是______________。
(2)若沉淀样品的质量为mg。装置C质量增加了ng,则沉淀中CuCO3的质量分数为_____________。
(3)通过查找资料得知,该浅绿色沉淀物可能是溶解度最小的碱式硫酸铜(化学式CuSO4·3Cu(OH)2)。请你设计一个实验,证明浊液中的浅绿色沉淀物中是否含有硫酸根离子的方法__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。则下列说法正确的是( )

A.Mg和Al的总质量为8 g
B.原稀硫酸溶液的物质的量浓度为5 mol·L-1
C.生成的H2在标准状况下的体积为11.2 L
D.NaOH溶液的物质的量浓度为5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题:
(1)完成下列化学方程式:
①将金属钠加入到硫酸铜溶液中的化学方程式:________
②漂白粉失效的化学方程式:________
③实验室制取氯气的化学方程式:________
(2)用化学方程式或离子方程式完成下列转化:
①Al3+→AlO2-→Al(OH)3________
②Fe(OH)2→Fe(OH)3________
③CO2→C________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生产、生活密切相关。下列有关说法不正确的是
A. 在燃煤中加生石灰以减少含硫化合物排放
B. 天然气运输时应悬挂如图所示的标志
C. 面粉生产车间应严禁烟火
D. 金属钠着火时使用泡沫灭火器或水灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知由![]() 溶液和稍过量的
溶液和稍过量的![]() 溶液制得的
溶液制得的![]() 胶体,当它跟
胶体,当它跟![]() 胶体相混合时,能析出
胶体相混合时,能析出![]() 和
和![]() 的混合沉淀,由此可知
的混合沉淀,由此可知
A. 该![]() 胶体进行电泳时,胶粒向阳极移动 B. 该
胶体进行电泳时,胶粒向阳极移动 B. 该![]() 胶体带负电荷
胶体带负电荷
C. 该![]() 胶粒带正电荷 D. 该
胶粒带正电荷 D. 该![]() 胶体是电解质
胶体是电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com