

���� ͼ��a���У����������£�ͭ��Ũ���ᷢ��������ԭ��Ӧ���ɶ�����������ͭ��ˮ�����������̼���ơ�S��C�з�Ӧ������������ƣ�������������������������ж�������ֱ���ſգ�Ӧ���ü�Һ���գ�
��1������1������ѹǿ�����װ�õ������ԣ�
����2������������л�ԭ�ԣ�����������������ж�������ֱ���ſգ����������Ը��������Һ�������Һ���գ�
����3��Na2S2O3��������Һ�в����ȶ����ڣ��ڼ����������ȶ����ڣ�
����4������Һ�л�ȡ���ʣ���Ҫ��������Ũ������ȴ�ᾧ�����˵ķ�����
��2����������ǿ�����ԣ���������ƾ��л�ԭ�ԣ����߷���������ԭ��Ӧ���������ơ���������
��ˮ�к��������ӣ�Ӱ����������ƻ�ԭ�Ե��жϣ�
��3���������֪��BaCrO4�������ܽ�ת��ΪCr2O2-7����Ԫ���غ㼰��֪����ʽ�ɵù�ϵʽ��2Ba2+��2BaCrO4��Cr2O2-7��3I2��6Na2S2O3��������ĵ�Na2S2O3���ù�ϵʽ������Һ��n��Ba2+������������c��Ba2+����
��� �⣺ͼ��a���У����������£�ͭ��Ũ���ᷢ��������ԭ��Ӧ���ɶ�����������ͭ��ˮ�����������̼���ơ�S��C�з�Ӧ������������ƣ�������������������������ж�������ֱ���ſգ�Ӧ���ü�Һ���գ�
��1������1�������Լ��鷽��Ϊ�رշ�Һ©����������D���ƿ�м�ˮ����û�����ܣ���K1���ر�K2���þƾ�����Բ����ƿ����D�����ܿ������ݲ�����ֹͣ���Ⱥ������γ�һ��ˮ����˵�����������ã�
�ʴ�Ϊ���رշ�Һ©����������D���ƿ�м�ˮ����û�����ܣ���K1���ر�K2���þƾ�����Բ����ƿ����D�����ܿ������ݲ�����ֹͣ���Ⱥ������γ�һ��ˮ����˵�����������ã�
����2������������л�ԭ�ԣ�����������������ж�������ֱ���ſգ����������Ը��������Һ�����������Ը��������Һ���գ����������Դ���̼�ᣬ�����ܺ�̼�����ơ�NaOH��Һ��Ӧ��������������Һ��̼��������Һ���գ�
��ѡ��ACD��
����3��Na2S2O3��������Һ�в����ȶ����ڣ��ڼ������������ȶ����ڣ�Ϊ�˷�ֹ��������Ʒ�����Ӧ��Ҫ������Һ��pH�ӽ���С��7��
�ʴ�Ϊ���ӽ���С��7��Na2S2O3��������Һ�в����ȶ����ڣ�
����4������Һ�л�ȡ���ʣ���Ҫ��������Ũ������ȴ�ᾧ�����˵ķ�����
�ʴ�Ϊ������Ũ������ȴ�ᾧ��
��2����������ǿ�����ԣ���������ƾ��л�ԭ�ԣ����߷���������ԭ��Ӧ���������ơ���������ᣬ��Ӧ����ʽΪNa2S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl��
��ˮ�к��������ӣ�Ӱ����������ƻ�ԭ�Ե��жϣ����Բ���ȷ��
�ʴ�Ϊ��Na2S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl������ȷ����Ϊ��ˮ�к��������ӣ�
��3���������֪��BaCrO4�������ܽ�ת��ΪCr2O2-7����Ԫ���غ㼰��֪����ʽ�ɵù�ϵʽ��2Ba2+��2BaCrO4��Cr2O2-7��3I2��6Na2S2O3�����ĵ�Na2S2O3Ϊ0.018L��0.01mol/L����n��Ba2+��=0.018L��0.01mol/L��$\frac{1}{3}$=0.00006mol������Һ��c��Ba2+��=$\frac{6��10{\;}^{-5}mol}{0.025L}$=2.4��10-3 mol•L-1��
�ʴ�Ϊ��2.4��10-3 mol•L-1��
���� ���⿼�������Ʊ�ʵ�鷽����ƣ�Ϊ��Ƶ���㣬�漰�����Լ��顢��ʵ��װ�ü�����ķ������ۡ����ʵķ����ᴿ��������ԭ��Ӧ�ζ���ע��ͼa�и���װ�õ����ü������ķ�Ӧ���ѵ���ȷ����3���и���������֮��Ĺ�ϵ����Ŀ�Ѷ��еȣ�


 ����Ӣ��ϵ�д�
����Ӣ��ϵ�д� ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
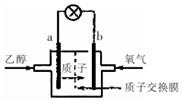 �Ҵ�ȼ�ϵ���в��û����������ܼ�����200������ʱ���磬����ܷ�ӦΪ��
�Ҵ�ȼ�ϵ���в��û����������ܼ�����200������ʱ���磬����ܷ�ӦΪ��| A�� | ��ع���ʱ���������صĸ���Ǩ�� | |
| B�� | ��ع���ʱ��������b���ص�������a�� | |
| C�� | a���Ϸ����ĵ缫��Ӧ�ǣ�C2H5OH+3H2O+12eһ=2CO2+12H+ | |
| D�� | -b���Ϸ����ĵ缫��Ӧ�ǣ�4H++O2+4eһ=2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.5 mol���ף�P4���ṹ��ͼ������2NA��P-P�� | |
| B�� | 23g������һ�����������������ã������߾���ʣ�࣬ת��NA������ | |
| C�� | 1mol/L��NH4��2SO4��Һ�У���SO2-4NA����NH+4����2NA�� | |
| D�� | ���³�ѹ��22.4L��CO2��һ����������������þ��Ӧ��ת��4NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

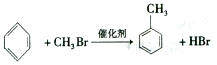 ����C���ʱ�����һ±����ֻ�����֣�
����C���ʱ�����һ±����ֻ�����֣� ��
�� $\stackrel{һ��������}{��}$
$\stackrel{һ��������}{��}$
 +
+ $��_{��}^{Ũ����}$H2O+
$��_{��}^{Ũ����}$H2O+
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
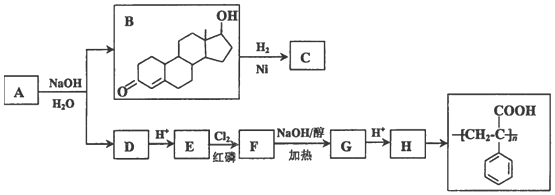
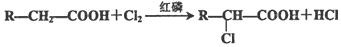
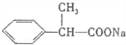 ��
��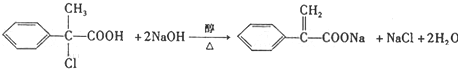 ��
��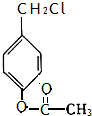 ��
��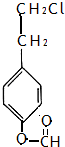 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com