
 对于如图所示的有机化合物的说法,正确的有①②③④⑦.
对于如图所示的有机化合物的说法,正确的有①②③④⑦.分析 ①卤代烃常温下呈液态,烃难溶于水;
②根据结构简式确定分子式;
③系统命名为:2,2-二甲基-1-氯-3-丁烯;
④该分子中含有四种氢原子,所以其核磁共振氢谱有4个吸收峰,氢原子个数之比为2:6:1:2;
⑤官能团名称为碳碳双键、氯原子;
⑥含有碳碳双键和氯原子,属于具有烯烃和氯代烃的性质;
⑦乙烯分子中所有原子共平面,根据乙烯结构判断共平面原子个数.
解答 解:①卤代烃常温下呈液态,卤代烃难溶于水,该物质为氯代烃,常温下为液态且难溶于水,故正确;
②根据结构简式确定分子式为C6H11Cl,故正确;
③系统命名为:2,2-二甲基-1-氯-3-丁烯,故正确;
④该分子中含有四种氢原子,所以其核磁共振氢谱有4个吸收峰,且氢原子个数之比为2:6:1:2,故正确;
⑤官能团名称为碳碳双键、氯原子,故错误;
⑥含有碳碳双键和氯原子,属于具有烯烃和氯代烃的性质,能发生加成反应、取代反应、氧化反应、还原反应、加聚反应,但不能发生消去反应,故错误;
⑦乙烯分子中所有原子共平面,根据乙烯结构判断共平面原子个数,碳碳单键可以旋转,则分子中最多有8个原子共平面,故正确;
故答案为:①②③④⑦.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确官能团及其性质关系、原子共面个数判断等知识点是解本题关键,难点是原子共平面个数判断,题目难度中等.


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:选择题
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCl | CO2 | 石灰水 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | NO2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |
| A. | ②③④ | B. | ①③④ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | M的化学性质活泼 | B. | L中的化学键是极性键 | ||
| C. | E能使紫色的石蕊试液变蓝 | D. | G是最活泼的非金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1LPH=0的硫酸溶液中,H+数为NA | |
| B. | 0.5mol 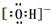 中含有的电子数为4.5NA 中含有的电子数为4.5NA | |
| C. | 7.8gNa2S与Na2O2的混合物中含有的阴离子数目为0.1NA | |
| D. | 0.1mol14N18O与3.1g13C18O的中子数均为1.7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤③①④② | B. | ⑤③①②④ | C. | ②④①③⑤ | D. | ②④③①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 表述1 | 表述2 | |
| A | 钠的金属性比铝强 | 钠原子核外电子数比铝少 |
| B | 金刚石的熔点高于晶体硅 | 原子半径Si大于C,键能Si-Si小于C-C |
| C | 离子晶体一般硬度较大,难压缩 | 离子晶体中阴、阳离子排列很有规律 |
| D | 相同条件下,分别完全燃烧等量的正丁烷和异丁烷,放出的热量相同 | 正丁烷与异丁烷互为同分异构体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com