
已知实验室可通过下列反应制取硫化氢气体:
FeS+H2SO4(稀)══FeSO4+H2S↑
为验证二氧化硫既有还原性又有氧化性,请用下面的试剂和仪器做实验。可选用的试剂:①盐酸 ②溴水 ③亚硫酸钠固体 ④硫化亚铁固体 ⑤品红试液 ⑥氢氧化钠溶液⑦浓硫酸
可选用的仪器装置如图所示。
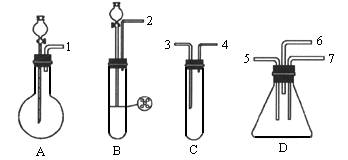
(1)按二氧化硫气流方向,用橡胶管(图中未画出)连接上述仪器,正确的连接顺序是(用导管口序号填空):________接________,________接________(或________)。
(2)在装置A、B、C中应加入的试剂是(用试剂序号填空):A________,B________,C________。
(3)表现二氧化硫氧化性实验所用的装置是上述装置中的________,实验中观察到的现象是________;表现二氧化硫的还原性实验所用的装置是上述装置中的________,实验中观察到的现象是________,其反应的离子方程式是________。
(4)整套装置最后的气体出口导管应连接________的装置,这样处理的理由是________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 已知A、B、D为中学常见的气体单质,甲、乙、丙、丁为常见的化合物,甲的水溶液呈碱性.它们之间有如下所示转化关系(部分产物及反应条件已略去)
已知A、B、D为中学常见的气体单质,甲、乙、丙、丁为常见的化合物,甲的水溶液呈碱性.它们之间有如下所示转化关系(部分产物及反应条件已略去)
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

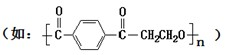 做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是
做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是查看答案和解析>>
科目:高中化学 来源: 题型:
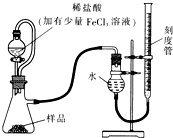 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
FeS+H2SO4(稀)══FeSO4+H2S↑
为验证二氧化硫既有还原性又有氧化性,请用下面的试剂和仪器做实验。可选用的试剂:①盐酸 ②溴水 ③亚硫酸钠固体 ④硫化亚铁固体 ⑤品红试液 ⑥氢氧化钠溶液⑦浓硫酸
可选用的仪器装置如图所示。
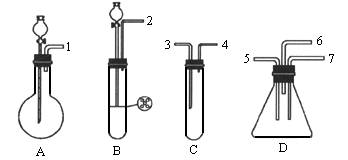
(1)按二氧化硫气流方向,用橡胶管(图中未画出)连接上述仪器,正确的连接顺序是(用导管口序号填空):________接________,________接________(或________)。
(2)在装置A、B、C中应加入的试剂是(用试剂序号填空):A________,B________,C________。
(3)表现二氧化硫氧化性实验所用的装置是上述装置中的________,实验中观察到的现象是________;表现二氧化硫的还原性实验所用的装置是上述装置中的________,实验中观察到的现象是________,其反应的离子方程式是________。
(4)整套装置最后的气体出口导管应连接________的装置,这样处理的理由是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com