
【题目】某药物中间体的合成路线如下![]() 下列说法正确的是()
下列说法正确的是()

A.对苯二酚在空气中能稳定存在
B.1mol该中间体最多可与11![]() 反应
反应
C.2,![]() 二羟基苯乙酮能发生加成、取代、缩聚反应
二羟基苯乙酮能发生加成、取代、缩聚反应
D.该中间体分子中含有1个手性碳原子
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述不正确的是
A.分子式为C4H8O2的酯有4种结构
B.主链含5个碳原子,有甲基、乙基2个支链的烷烃有3种
C.丙烯分子中最多有7个原子共平面
D.乙烯和溴的四氯化碳溶液反应生成1,2二溴乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四元轴烯 t、苯乙烯 b 及立方烷 c 的分子式均为 C8H8。下列说法正确的是

A.b 的同分异构体只有 t 和 c 两种
B.t、b、c 中只有 t 的所有原子可以处于同一平面
C.t、b、c 的二氯代物均只有三种
D.t 和b 能使酸性 KMnO4 溶液褪色而c不能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组所做的石蜡油(17个碳原子以上的烷烃)分解实验如图所示。下列有关说法正确的是
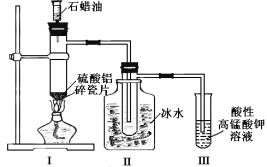
A.装置II中逸出的气体通入高锰酸钾溶液,发生加成反应
B.石蜡油分解生成的气体中只有烯烃
C.十八烷完全分解为乙烷和最多乙烯时,二者物质的量之比为1:8
D.装置I中硫酸铝和碎瓷片都是催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铅蓄电池放电时的反应为![]() 。某兴趣小组用铅蓄电池电解饱和食盐水的装置如下图所示,下列说法正确的是
。某兴趣小组用铅蓄电池电解饱和食盐水的装置如下图所示,下列说法正确的是
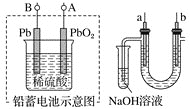
A.铅蓄电池A极应与U形管中a极连接
B.a、b两极均可用金属铁作电极
C.a电极用铁作电极,b电极用石墨作电极
D.实验结束后可将U形管、试管中的溶液倒入下水道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡妥油(D)用作香料的原料,它可由A合成得到:

A. 从B到C的反应是消去反应
B. D分子中所有碳原子一定共面
C. 等物质的量的B分别与足量的Na、NaHCO3反应,产生的气体的物质的量前者大于后者
D. 若A是由2-甲基-1,3-丁二烯和丙烯酸(CH2=CHCOOH)加热得到的,则该反应的类型属于加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,反应CCl4(g)+H2(g)![]() CHCl3(g)+HCl(g) ,可使CCl4(沸点77 ℃)转化为重要的化工原料CHCl3(沸点61.2 ℃),可减少其对臭氧层的破坏。(已知:该反应的副反应会生成CH2Cl2、CH3Cl和CH4等)
CHCl3(g)+HCl(g) ,可使CCl4(沸点77 ℃)转化为重要的化工原料CHCl3(沸点61.2 ℃),可减少其对臭氧层的破坏。(已知:该反应的副反应会生成CH2Cl2、CH3Cl和CH4等)
(1)CH4与Cl2反应时,每生成1molCCl4(g)或1molCHCl3(g)的焓变分别是△H1和△H2;H2在Cl2中燃烧,每生成1molHCl(g)产生的焓变为△H3,则:CCl4(g)+H2(g)![]() CHCl3(g)+HCl(g)的△H=_____(用含有△H1、△H2和△H3的算式表示)
CHCl3(g)+HCl(g)的△H=_____(用含有△H1、△H2和△H3的算式表示)
(2)在密闭容器中,CCl4+H2![]() CHCl3+HCl达到平衡状态后,测得如下数据(假设不考虑副反应)。
CHCl3+HCl达到平衡状态后,测得如下数据(假设不考虑副反应)。
实验序号 | 温度/℃ | 初始CCl4浓度/(mol·L-1) | 初始H2浓度/(mol·L-1) | CCl4的平衡转化率 |
1 | 110 | 0.8 | 1.2 | α1 |
2 | 110 | 1 | 1 | 50% |
3 | 100 | 1 | 1 | α3 |
①实验1中,CCl4的转化率α1_____50%(填“大于”“小于”或“等于”)。
②实验2中,反应进行到10h时达到平衡,在这10h内,H2的平均反应速率为_____mol· L-1·min-1。
③110 ℃时,该反应的化学平衡常数的数值为________。
④实验3中,α3的值________。
A. 等于50% B.大于50% C.小于50% D.依题所给信息无法判断
(3)120 ℃时,分别进行H

①图中表示H2起始浓度为2mol·L-1CHCl3的百分含量的变化曲线是____(填字母)。
②依图可知,有利于提高CCl4的消耗百分率和产物中CHCl3的百分含量H2的起始浓度应该为________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒容密闭容器中发生某化学反应2A(g)![]() B(g)+C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的初始浓度都为0,反应物A的浓度(mol·L-1)随时间(min)的变化如图的示:试回答下列问题:
B(g)+C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的初始浓度都为0,反应物A的浓度(mol·L-1)随时间(min)的变化如图的示:试回答下列问题:
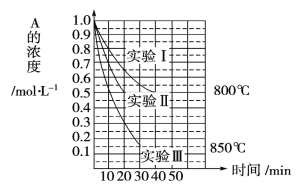
(1)在800℃时该反应的化学平衡常数K=_____。
(2)在实验Ⅰ中,反应在20min至40min内A的化学反应速率为_________。
(3)实验Ⅱ和实验Ⅰ相比,可能隐含的反应条件是_____。
(4)根据实验Ⅲ和实验Ⅰ的比较,可推测该反应降低温度,平衡向_____(填“正”或“逆”)反应方向移动,该正反应是__________(填“放热”或“吸热”)反应。
(5)与实验Ⅰ相比,若实验Ⅰ中的A的初始浓度改为0.8mol·L-1,其他条件不变,则达到平衡时所需用的时间_____实验Ⅰ(填“等于”、“大于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(选用)CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2 而得到。如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI一淀粉溶液中阳极周围变蓝色,则下列说法正确的是

A.若a极变红,则在Pt电极上:2I--2e-=I2碘遇淀粉变蓝
B.若b极变红,在Pt电极上:4OH--4e-=2H2O+O2,O2将I-氧化为I2,碘遇淀粉变蓝
C.若a极变红,在Cu电极上:开始Cu+I--e-=CuI,一段时间后2I--2e-=I2,碘遇淀粉变蓝
D.若b极变红,在Cu极上:Cu-2e-=Cu2+,Cu2+显蓝色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com