
| A. | ①②③④⑤⑥ | B. | ①②③④⑤⑧ | C. | ①②③⑥⑧ | D. | ②⑥⑦ |
分析 钠的密度小于水、熔点较小,钠和水反应生成氢氧化钠和氢气且放出大量热,氢氧化钠和硫酸铜发生复分解反应生成氢氧化铜和硫酸钠,涉及的反应方程式为2Na+2H2O=2NaOH+H2↑、2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
解答 解:①钠的密度小于水,所以钠会浮于液面上,故正确;
②钠的熔点较低,钠和水反应放出的热量而使钠熔化成小球,故正确;
③钠的性质很活泼,易和水剧烈反应生成氢气,所以发出嘶嘶的响声,放出气体,故正确;
④钠和水反应生成的氢氧化钠再与硫酸铜发生复分解反应生成氢氧化铜蓝色沉淀,所以有蓝色沉淀产生,故正确;
⑤钠和水反应放出的大量热而使氢氧化铜分解生成黑色的不溶性氧化铜,则周围蓝色沉淀部分变黑,故正确;
⑥钠的性质很活泼,先和水反应,而不是和铜离子发生置换反应,所以不会析出大量红色的铜,故错误;
⑦钠的密度小于溶液密度,所以会浮在液面上,故错误;
⑧钠和水反应生成的氢气而使钠受力不均导致钠四处游动,逐渐变小直至消失,故正确;
故选B.
点评 本题考查钠与硫酸铜溶液混合现象,明确钠及氢氧化钠性质是解本题关键,要根据钠的物理性质及化学性质分析化学现象,易错点是化学用语的正确使用,题目难度不大.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2Na:两个钠元素 | |
| B. | 2OH-:两个氢氧根离子 | |
| C. | $\stackrel{+2}{M}$g:镁元素的化合价为+2价 | |
| D. | NO2:一个二氧化氮分子含有两个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| Ⅰ | Cu、稀HNO3 | H2O | |
| Ⅱ | NaOH固体、浓氨水 | NH3 | |
| Ⅲ | 镁铝合金、足量NaOH溶液 | H2 | H2O |
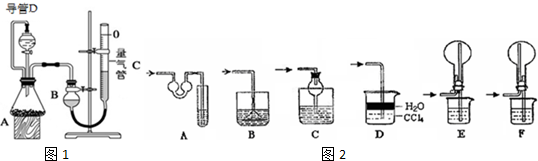
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 376.6mL |
| ② | 1.0g | 10.0mL | 364.7mL |
| ③ | 1.0g | 10.0mL | 377.0mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 赤铁矿:Fe3O4 | B. | 铜绿:Cu2(OH)2CO3 | C. | 磁铁矿:Fe2O3 | D. | 明矾:2KAl(SO4)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 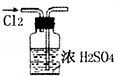 干燥Cl2 | |
| B. |  配制90ml 0.1mol•L-1硫酸溶液 | |
| C. |  分离沸点相差较大的互溶液体混合物 | |
| D. |  分离互不相溶的两种液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com