
下列关于铁的叙述正确的是
①铁能被磁铁吸引,但纯铁比含杂质的铁易被腐蚀
②在人体的血红蛋白中含有铁元素
③铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧
④铁与强氧化剂硝酸反应的产物只有一种是Fe(NO3)3
⑤不能通过化合反应制得FeCl2和Fe(OH)3
A.①③ B.②③ C.②⑤ D.④⑤
科目:高中化学 来源:2016届重庆市高三上学期10月月考理综化学试卷(解析版) 题型:选择题
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为 CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则消耗氧气的体积2.24L
C.电池反应的化学方程式为:CH3CHO+O2=CH3COOH+H2O
D.正极上发生的反应是:O+4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省泰州市姜堰区高二上学期期中选修化学试卷(解析版) 题型:选择题
制取水煤气的反应为C(s)+H2O(g)  CO(g)+H2(g) △H > 0,欲提高反应的速率和C(s)的转化率,可采用的措施为
CO(g)+H2(g) △H > 0,欲提高反应的速率和C(s)的转化率,可采用的措施为
A.降温 B.增大水蒸气的浓度 C.增大C(s)的量 D.增大压强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第一次月考化学试卷(解析版) 题型:选择题
工业生产水煤气的反应为:C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.4kJ·mol-1下列判断正确的是
CO(g)+H2(g) ΔH=+131.4kJ·mol-1下列判断正确的是
A.反应物能量总和大于生成物能量总和
B.CO(g)+H2(g) C(s)+H2O(g) ΔH=+131.4kJ·mol-1
C(s)+H2O(g) ΔH=+131.4kJ·mol-1
C.水煤气反应中,生成1 mol H2(g)吸收131.4 kJ热量
D.水煤气反应中生成1体积CO(g)吸收131.4 kJ热量
查看答案和解析>>
科目:高中化学 来源:2016届福建省大田市高三上学期第一次月考化学试卷(解析版) 题型:实验题
ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂.已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与纯净的氯气反应 2NaClO2+Cl2═2ClO2+2NaCl。如图1是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略).其中E中盛有CCl4液体。
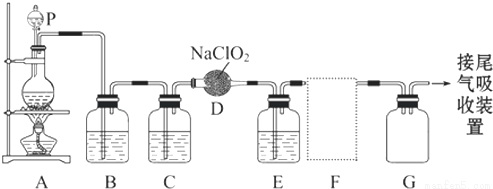
(1)仪器P的名称是
(2)写出装置A中烧瓶内发生反应的化学方程式:
(3)E装置中所盛试剂的作用是
(4)F处应选用的收集装置是图2 (填序号),其中与E装置导管相连的导管口是图2 (填接口字母).
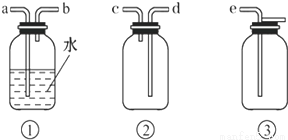
(5)以下是尾气吸收装置,能用于吸收多余ClO2气体,并能防止倒吸的装置的是如图3的
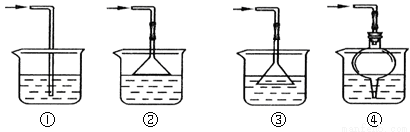
A.①② B.②③ C.③④ D.②④
(6)若用100mL 2mol•L﹣1的浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量是 (填序号).
A.>0.1mol B.0.1mol C.<0.1mol D.无法判断.
(7)ClO2也可由NaClO3在H2SO4溶液存在下与Na2SO3反应制得.请写出反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列各组离子在常温下一定能大量共存的是
A.pH=0的无色溶液中:Cl-、Na+、SO42-、Fe2+
B.在c(H+)/c( OH-) =1012的溶液中:NH4+、NO3-、K+、Cl-
C.加入铝粉能放出H2的溶液中:Mg2+、NH4+、NO3-、Cl-
D.含有大量Fe3+的溶液中:Al3+、SCN-、Br-、Na+
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(8分)某强碱性溶液中可能含有的离子是K+、NH4+、Al3+、AlO2﹣、SO42﹣、SiO32﹣、CO32﹣、Cl﹣中的某几种离子,现进行如下实验:
①取少量的溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成.
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
(1)肯定不存在的离子是 .
(2)写出步骤②中生成沉淀和气体的反应的离子方程式: ; 。
(3)已知一定量的原溶液中加入5mL 0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g,则原溶液中是否含有Cl﹣? (填“有”或“无”).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期半期考试化学试卷(解析版) 题型:推断题
已知可由乙烯合成高分子材料G 。
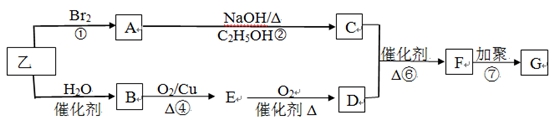
F的质谱图中最大质荷比为86, 其C、H、O的原子个数之比为2:3:1,F在酸性条件下水解可生成碳原子数相同的两种有机物D和E。请回答下列问题:
(1)B的分子式为 ,F分子含氧官能团的名称为 。
(2)E的结构简式为 ,G的结构简式为 。
(3)反应①、⑥的反应类型均是 。
(4)反应②的化学方程式为 。
(5)在F的同分异构体中,核磁共振氢谱有三个峰,三个峰的面积之比为1:1:1,任意写出其中一种满足上述条件的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上第一次月考化学试卷(解析版) 题型:填空题
(一)向一容积不变的密闭容器中充入一定量A和B,发生如下反应: x A(g) +2B(s) y C(g); △H <0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
y C(g); △H <0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
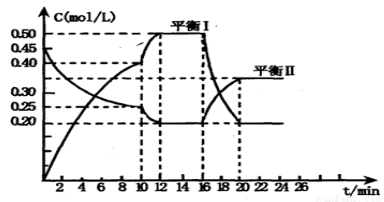
(1)0~l0min容器内压强____ (填“变大”,“不变”或“变小”)
(2)推测第l0min引起曲线变化的反应条件可能是 ;第16min引起曲线变化的反应条件可能是____ ;
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(3)若平衡I的平衡常数为K1,平衡Ⅱ平衡常数为K2,则K1 __________ K2(填“>”“=”或“<”)
(二) 尿素是蛋白质代谢的产物,也是重要的化学肥料。工业合成尿素反应如下:
2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
(1)在一个真空恒容密闭容器中充入CO2和NH3发生上述反应合成尿素,恒定温度下混合气体中的氨气含量如图所示。

A点的正反应速率v正(CO2)_______B点的逆反应速率v逆(CO2)(填“>”、“<”或“=”);氨气的平衡转化率为________________________。
(2)氨基甲酸铵是合成尿素的一种中间产物。将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:2NH3(g)+CO2(g)  NH2COONH4(s) 关于上述反应的平衡状态下列说法正确的是________________
NH2COONH4(s) 关于上述反应的平衡状态下列说法正确的是________________
A.分离出少量的氨基甲酸铵,反应物的转化率将增大
B.平衡时降低体系温度,CO2的体积分数下降
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高氨基甲酸铵的产率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com