
【题目】CuCl是应用广泛的有机合成催化剂,可从黄铜矿(主要成分为CuFeS2)中制取。
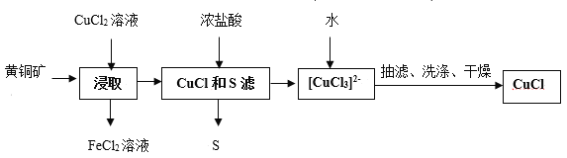
已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)(无色溶液)
[CuCl3]2-(aq)(无色溶液)
下列叙述错误的是( )
A.浸取中的主要反应为CuFeS2+3CuCl2=4CuCl+FeCl2+2S
B.浸取所得到的FeCl2溶液,可用来腐蚀覆在绝缘板上的铜箔制造印刷电路板
C.加水有利于CuCl(s)+2Cl(aq)-![]() [CuCl3]2-(aq)平衡逆向移动,析出CuCl
[CuCl3]2-(aq)平衡逆向移动,析出CuCl
D.为提高产率和纯度,可采用乙醇洗涤、真空干燥
【答案】B
【解析】
黄铜矿和氯化铜反应生成氯化亚铜、氯化亚铁和硫单质,CuCl和盐酸反应生成[CuCl3]2-,加水稀释利用平衡移动原理CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq),平衡逆向移动,生成氯化亚铜。
[CuCl3]2-(aq),平衡逆向移动,生成氯化亚铜。
A选项,根据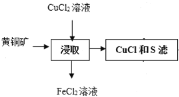 ,浸取中的主要反应为CuFeS2+3CuCl2= 4CuCl+FeCl2+2S,故A正确;
,浸取中的主要反应为CuFeS2+3CuCl2= 4CuCl+FeCl2+2S,故A正确;
B选项,浸取所得到的FeCl2溶液和铜不反应,故B错误;
C选项,加水,反应物浓度减小更多,CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)平衡逆向移动,析出CuCl,故C正确;
[CuCl3]2-(aq)平衡逆向移动,析出CuCl,故C正确;
D选项,因CuCl微溶于水,难溶于乙醇,在空气中易被氧化,为提高产率和纯度,因此采用乙醇洗涤、真空干燥CuCl,故D正确;
综上所述,答案为B。


科目:高中化学 来源: 题型:
【题目】观察下列几个装置示意图,有关叙述不正确的是( )
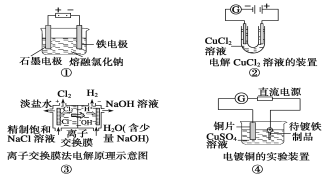
A.装置①工业上可用于生产金属钠,电解过程中石墨电极产生氯气,此法也可用于生产活泼金属镁、铝等
B.装置②中随着电解的进行右边电极会产生红色的铜,并且电流计示数不断变小
C.装置③中的离子交换膜具有很强的选择性,只允许某类离子(如Na+)通过
D.装置④的待镀铁制品应与电源负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。[制取氨气的反应原理:2NH4Cl + Ca(OH)2 ![]() CaCl2 + 2NH3↑+2H2O ]
CaCl2 + 2NH3↑+2H2O ]
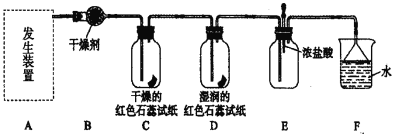
(实验探究)
(1)利用上述原理,实验室制取氨气应选用下图中________发生装置进行实验。

(2)B装置中的干燥剂可选用________。
(3)用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为________ L。(NH4Cl的摩尔质量为53.5g·mol—1)
(4)气体通过C、D装置时,试纸颜色会发生变化的是____(填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_______。
(6)F装置中倒置漏斗的作用_______。
(拓展应用)
(7)某同学用如图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有________性质(填序号)。
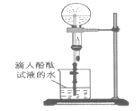
a 还原性 b 极易溶于水 c 与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮:8NH3 + 6NO2 =7N2 + 12H2O
该反应中氨气体现________(填“氧化性”或“还原性”)。请你列举出氨气的另一种用途________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是重要的催化剂和化工原料,工业上制备Cu2O的主要反应如下:
Ⅰ.C(s)+CO2(g)![]() 2CO(g) ΔH=+172.5kJ·mol-1
2CO(g) ΔH=+172.5kJ·mol-1
Ⅱ.CO(g)+2CuO(s)![]() Cu2O(s)+CO2(g) ΔH=-138.0 kJ·mol-1
Cu2O(s)+CO2(g) ΔH=-138.0 kJ·mol-1
请回答:
(1)一定温度下,向5L恒容密闭容器中加入1molCO和2molCuO,发生反应Ⅱ,2min时达到平衡,测得容器中CuO的物质的量为0.5mol。
①0-2min内,用CO表示的反应速率v(CO)=___。
②CO2的平衡体积分数φ=___。
(2)向5L密闭容器中加入1molC和1molCO2,发生反应Ⅰ。CO2、CO的平衡分压(p)与温度(T)的关系如图所示(平衡分压=物质的量分数×总压强)。
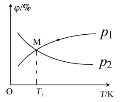
①能表示CO2的平衡分压与温度关系的曲线为___(填"p1”或“p2”),理由是___。
②温度为T1时,该反应的平衡常数K=___;温度升高,K___(填“变小”、“变大”或“不变”)
③实验测得,v正=v(CO2)消耗=k正c(CO2),v逆=v(CO)消耗=k逆c2 (CO),k正、k逆为速率常数,受温度影响,则温度为T1时,k正/k逆=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)在鼓泡反应器中通入含有SO2和NOx的烟气,反应温度为323K,NaClO2碱性溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如表。
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/mol·L1 | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2碱性溶液脱硝(NO)过程中主要反应的离子方程式:____。增加压强,NO的转化率___(填“提高”“不变”或“降低”)
②由实验结果可知,脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___。
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压px如图所示。
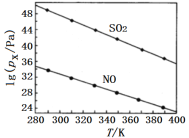
由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均___(填“增大”“不变”或“减小”)。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述不正确的是
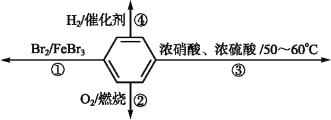
A.反应①为取代反应,有机产物与水混合时分层并处于下层
B.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C.反应③为取代反应,可用水浴加热控制温度
D.反应④中1 mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ4种类型,苏丹红Ⅰ的分子结构如图1所示。
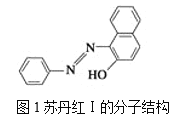
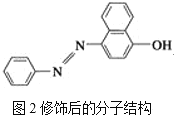
苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会____(填“增大”或“减小”),原因是__________________。
(2)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的结构式为__________,第二种配合物的结构式为_____。
(3)Ag+能与NH3、S2O32-、CN等形成配位数为2的配合物。
利用AgNO3和氨水可配制[Ag(NH3)2]OH溶液,在[Ag(NH3)2]OH中存在的化学键的类型有_____(填字母)。
A 离子键 B 金属键 C 配位键 D 非极性键 E 极性键
(4)NO3-中N原子的杂化轨道类型是____,空间构型为_____。写出一种与NO2-,SO2互为等电子体的短周期元素单质分子的化学式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃烧法是确定有机物分子式常用的方法:在电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成。若实验中所取样品A只含C、H、O三种元素中的两种或三种,准确称取0.92 g样品,经充分反应后,测得生成1.76 gCO2和1.08 g水;回答下列问题:
(1)样品A的实验式为____________。能否根据A的实验式确定A的分子式_______ (填“能”或“不能”),若能,则A的分子式是____________________ (若不能,则此空不填)。
(2)样品A不能与金属钠反应,则其结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多,该化合物具有如下性质:
(1)1molX与足量的金属钠反应产生1.5 mol气体
(2)X与醇或羧酸在浓H2SO4和加热的条件下均生成有香味的产物
(3)X在一定程度下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应
根据上述信息,对X的结构判断正确的是 ( )
A.X中肯定有碳碳双键
B.X中可能有三个羟基和一个-COOR官能团
C.X中可能有三个羧基
D.X中可能有两个羧基和一个羟基
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com