
A、 |
B、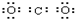 |
C、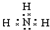 |
D、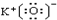 |
 ,故A错误;
,故A错误; ,故B错误;
,故B错误;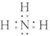 ,故C正确;
,故C正确;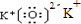 ,故D错误;
,故D错误;

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
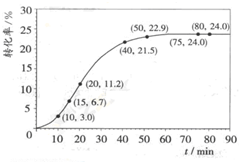 甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)?HCOOH(l)+CH3OH(l);△H>0
甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)?HCOOH(l)+CH3OH(l);△H>0| 组分 | HCOOCH3 | H2O | HCOOH | CH3OH |
| 物质的量/mol | 1.00 | 1.99 | 0.01 | 0.52 |
| 反应时间范围/min | 0~5 | 10~15 | 20~25 | 30~35 | 40~45 | 50~55 | 75~80 |
| 平均反应速率/(10-3mol?min-1) | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |
| c(HCOOH)?c(CH3OH) |
| c(HCOOCH3)?c(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入稀释100倍后,两溶液的pH相同 |
| B、加入NaOH固体恰好中和后,两溶液的pH相同 |
| C、加入足量的小苏打固体充分反应后,两溶液中产生的CO2一样多 |
| D、分别加入足量的锌粉充分反应,反应开始时两酸产生H2的反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、把X和Y组成的合金放于潮湿的空气中,X先被腐蚀 |
| B、X原子最外层电子数比Y原子最外层电子数少 |
| C、X能从Y的盐溶液中把Y置换出来 |
| D、电解X和Y的盐混合液,阴极先析出Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀 |
| B、在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 |
| C、向AlCl3溶液中滴加氨水,产生白色沉淀;再加入NaHSO4溶液,沉淀消失 |
| D、除去FeCl2中少量的FeBr2,加入适量氯水;再加四氯化碳萃取分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
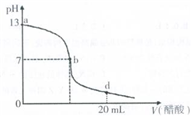
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=9的氨水溶液稀释1000倍 |
| B、pH=9的烧碱溶液稀释1000倍 |
| C、pH=5的盐酸溶液稀释1000倍 |
| D、pH=5的氯化铵溶液稀释1000倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯锌与稀硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 |
| B、甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为:CH3OH+6OH-+6e-═CO2+5H2O |
| C、在铁上镀铜时,金属铜作阴极 |
| D、电解精炼铜时,电解质溶液中铜离子浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸与氢氧化钾溶液 |
| B、稀硫酸与氢氧化钡溶液 |
| C、硫酸氢钠溶液与氢氧化钠溶液 |
| D、盐酸与氨水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com