
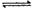 Fe(s)+CO2(g) ��H=akJ��mol(a>0)�����¶���K=0.263�������йظ÷�Ӧ��˵����ȷ����
Fe(s)+CO2(g) ��H=akJ��mol(a>0)�����¶���K=0.263�������йظ÷�Ӧ��˵����ȷ����| A���ﵽ��ѧƽ��״̬ʱ����c (CO)="0.100" mol��L����c��CO2��="0.0263" mol/L |
| B����Ҫ���CO��ת���ʣ���Ӧ�ü����ʵ��Ĺ���FeO |
| C����������ѹǿ����ʱ��仯��������жϸ÷�Ӧ�Ѵﵽ��ѧƽ��״̬ |
| D��������56 g Fe�������յ�����С��a kJ |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
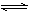 NH3��H2O
NH3��H2O 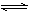 NH
NH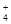 ��OH��
��OH�� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

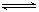 XeF4(g)��F2(g)��
XeF4(g)��F2(g)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ı���������Ӧ���ת��������ƽ�ⳣ��Ҳһ������ |
B����Ӧ2NO2(g)  N2O4(g) ��H��0�������¶ȸ÷�Ӧƽ�ⳣ������ N2O4(g) ��H��0�������¶ȸ÷�Ӧƽ�ⳣ������ |
| C�����ڸ������淴Ӧ���¶�һ��ʱ���������淴Ӧ��ƽ�ⳣ����� |
D��ƽ�ⳣ��Ϊ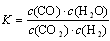 �ķ�Ӧ����ѧ����ʽΪCO2��H2 �ķ�Ӧ����ѧ����ʽΪCO2��H2 CO��H2O CO��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
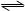 2C+3D�Ļ�ѧ��Ӧ�����뻯ѧƽ������������ı�(�Ƚ��º��ѹ)���仯�����,�ɴ˿����ƶ�
2C+3D�Ļ�ѧ��Ӧ�����뻯ѧƽ������������ı�(�Ƚ��º��ѹ)���仯�����,�ɴ˿����ƶ�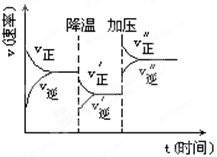
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH(g)��H2O(g) ��H����49.0kJ/mol
CH3OH(g)��H2O(g) ��H����49.0kJ/mol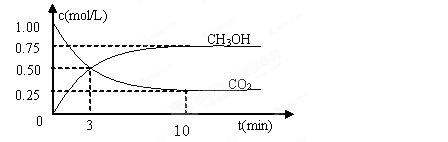
| A�������¶� | B������He(g)��ʹ��ϵѹǿ���� |
| C����H2O(g)����ϵ�з��� | D���ٳ���1mol CO2��3mol H2 H2 |
 ͬ�����ʵ�v����v���Ĺ�ϵ: v�� v�� (���������)
ͬ�����ʵ�v����v���Ĺ�ϵ: v�� v�� (���������)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
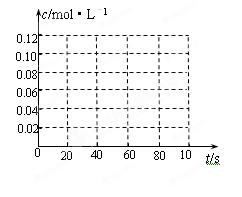
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 4C(g)
4C(g)  H ��0 �ﵽƽ��ʱ��c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L����ȷ��B����ʼŨ��c(B)��ȡֵ��Χ�� �����ı��������´ﵽƽ�����ϵ��C�����������������д�ʩ���е���
H ��0 �ﵽƽ��ʱ��c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L����ȷ��B����ʼŨ��c(B)��ȡֵ��Χ�� �����ı��������´ﵽƽ�����ϵ��C�����������������д�ʩ���е��� �鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com