
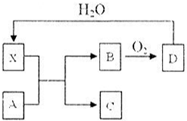
 铁、铜及其化合物应用广泛,如FeCl3可用作印刷电路铜板腐蚀剂和外伤止血剂等;CuCl2可用作消毒剂、媒染剂、催化剂;硫酸铁可用作电化浸出黄铜矿精矿工艺.
铁、铜及其化合物应用广泛,如FeCl3可用作印刷电路铜板腐蚀剂和外伤止血剂等;CuCl2可用作消毒剂、媒染剂、催化剂;硫酸铁可用作电化浸出黄铜矿精矿工艺.| 催化剂 |
| 催化剂 |
| 64x+128y |
| 80x+144y |
| 85 |
| 100 |
| x |
| y |
| 7 |
| 5 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硝酸保存在棕色细口瓶中 |
| B、液溴用水封保存 |
| C、少量金属钠保存在煤油中 |
| D、烧碱溶液保存在带玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
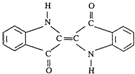
| A、靛蓝由碳、氢、氧、氮四种元素组成 |
| B、它的分子式是C16H10N2O2 |
| C、它是芳香族有机物 |
| D、该物质是高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
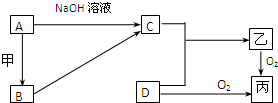 已知A、B为常见的金属单质,C、D为常见的非金属单质,甲、乙、丙为三种常见的化合物,它们之间的相互转化关系如下图所示(部分产物及反应条件没有列出):
已知A、B为常见的金属单质,C、D为常见的非金属单质,甲、乙、丙为三种常见的化合物,它们之间的相互转化关系如下图所示(部分产物及反应条件没有列出):查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③⑤ | B、②③④ |
| C、①③④ | D、①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
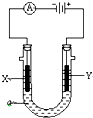 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com