
【题目】以甲醛和苯酚为主要原料,经如图所示系列转化可合成酚醛树脂和重要有机合成 中间体 D(部分反应条件和产物略去):
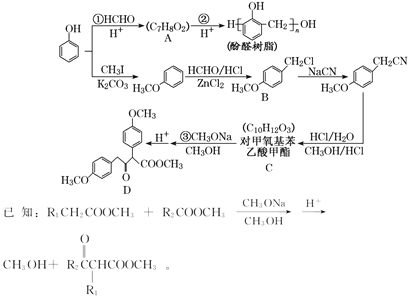
(1)CH3OH 的名称为_____。
(2)C 中所含官能团的名称是_____。
(3)反应②的化学方程式是_____。
(4)下列关于 A 的性质,能反映支链对苯环结构产生影响的是_____(填字母)。
a.能与氢氧化钠溶液反应 b.能使酸性高锰酸钾溶液褪色 c.稀溶液中加浓溴水产生沉淀
(5)E(C8H10O2)与 B 的水解产物互为同分异构体,1 mol E 可与 2 mol NaOH 反应,其核磁共振氢谱显示有 3 种峰且峰面积之比为 3∶1∶1,符合条件的 E 共有_____种。
(6) 完成下面以 CH3OH 和 CH3ONa 为 原 料 ( 其 他 无 机 试 剂 任 选 ) 制 备 化 合 物CH3COCH2COOCH3 的合成路线。 CH3OH――△→… ___________________________________________
【答案】甲醇 酯基、醚键 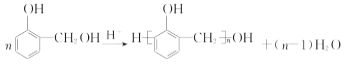 c 4
c 4 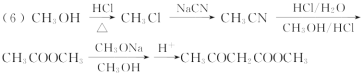
【解析】
根据合成路线流程图,反应①中苯酚与甲醛反应生成A(C7H8O2),该反应属于加成反应,根据酚醛树脂的结构可知A为![]() ,其他物质根据所给结构及已知条件对物质的反应进行分析解答。
,其他物质根据所给结构及已知条件对物质的反应进行分析解答。
(1) CH3OH的名称为甲醇;
(2) C是对甲氧基苯乙酸甲酯,所含官能团有酯基、醚键;
(3) 反应②为![]() 发生缩聚反应生成
发生缩聚反应生成![]() 的反应,反应的方程式为
的反应,反应的方程式为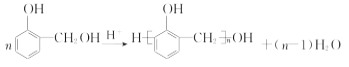 ;
;
(4) A为![]() 。a.分子中含有酚羟基,能与氢氧化钠溶液反应,与苯环上的支链无关,故a不选;b. 分子中含有酚羟基,能被酸性高锰酸钾溶液氧化为粉红色的物质,与苯环上的支链无关,故b不选;c.稀溶液中加浓溴水产生沉淀,与苯环上的羟基有关,故c选,故选c;
。a.分子中含有酚羟基,能与氢氧化钠溶液反应,与苯环上的支链无关,故a不选;b. 分子中含有酚羟基,能被酸性高锰酸钾溶液氧化为粉红色的物质,与苯环上的支链无关,故b不选;c.稀溶液中加浓溴水产生沉淀,与苯环上的羟基有关,故c选,故选c;
(5) 1molE(C8H10O2)可与2molNaOH反应,说明含有2mol羟基,其核磁共振氢谱显示有3种峰且峰面积之比为3:1:1,符合条件的E有![]() 、
、![]() 、
、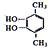 、
、![]() ,共4种;
,共4种;
(6)以CH3OH为原料制备化合物CH3COCH2COOCH3。根据题干中B到D的转化过程,可以首先将CH3OH转化为CH3Cl,再转化为CH3CN,水解为乙酸甲酯,最后根据题干信息转化即可。合成路线为![]() 。
。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】下列方程式正确的是
A. 小苏打与盐酸反应的离子方程式:CO32- + 2H+= CO2↑+H2O
B. 乙烯与氯化氢加成的化学方程式:CH2=CH2+HCl![]() CH3=CH2Cl
CH3=CH2Cl
C. 碳酸钾在水中的电离方程式: K2CO3![]() K++CO32-
K++CO32-
D. 醋酸钠水解的离子方程式:CH3COO- + H2O ![]() CH3COOH + OH-
CH3COOH + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.催化剂可以改变反应的焓变
B.放热反应不需加热即可发生
C.强电解质都是可溶性化合物
D.若某反应的H和S均为正值,则其可能在高温时自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从石油和煤中提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的结构简式_______________,B的结构简式_________________;
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:_____________;反应类型:___________。
(3)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式: ______________________ 反应类型:___________。
(4)等质量的A、B完全燃烧时消耗O2的物质的量________(填A>B、A<B或A=B”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两种溶液中分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-这6种离子中的3种(两种溶液中的离子不重复),已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
A.Cu2+、H+、Cl-B.K+、OH-、CO32-
C.CO32-、OH-、Cl-D.K+、H+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaOH、MgCl2、A1C13三种固体组成的混合物溶于足量水后得1.16g白色沉淀。在所得的浊液中逐滴加入1mo1·L-1HC1溶液,加入HC1溶液的体积与生成沉淀的质量关系如图所示,试回答:
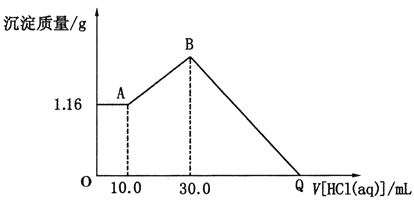
(1)写出混合物溶于水时发生反应的离子方程式:_____________________________。
(2)写出AB段反应的离子方程式:_______________________________。
(3)原混合物中NaOH的物质的量是多少?(写出计算过程) ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处于另一周期。C、B可按原子个数比2∶1和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。D的周期序数等于D原子最外层电子数。E原子半径是同周期中最小的(除稀有气体外)。根据以上信息回答下列问题:
(1)A、B、C、D、E五种元素的原子半径由小到大的顺序是__________________ (用元素符号填写),其中D的最高价氧化物是________氧化物(填“酸性”“碱性”或“两性”)。
(2)乙物质中存在的化学键类型是________。
(3)化合物乙的电子式为________。
(4)写出C与D分别对应的最高价氧化物的水化物反应的离子方程式:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com