



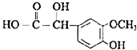
 ��FΪ
��FΪ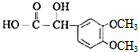 ���Ա�G�Ľṹ��E�ķ���ʽ����֪EΪOHC-COOH����B����������ˮ��Һ�����������·���ˮ�ⷴӦ����CΪHOCH2CH2OH��DΪOHC-CHO��D�в���ȩ������������E��J��һ�������·�����Ϣii�����ȷ�Ӧ����KΪ
���Ա�G�Ľṹ��E�ķ���ʽ����֪EΪOHC-COOH����B����������ˮ��Һ�����������·���ˮ�ⷴӦ����CΪHOCH2CH2OH��DΪOHC-CHO��D�в���ȩ������������E��J��һ�������·�����Ϣii�����ȷ�Ӧ����KΪ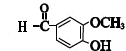 �������Ϣiii�������صķ���ʽ����֪�����صĽṹ��ʽΪ��
�������Ϣiii�������صķ���ʽ����֪�����صĽṹ��ʽΪ�� ���ݴ˽��
���ݴ˽�� ��FΪ
��FΪ ���Ա�G�Ľṹ��E�ķ���ʽ����֪EΪOHC-COOH����B����������ˮ��Һ�����������·���ˮ�ⷴӦ����CΪHOCH2CH2OH��DΪOHC-CHO��D�в���ȩ������������E��J��һ�������·�����Ϣii�����ȷ�Ӧ����KΪ
���Ա�G�Ľṹ��E�ķ���ʽ����֪EΪOHC-COOH����B����������ˮ��Һ�����������·���ˮ�ⷴӦ����CΪHOCH2CH2OH��DΪOHC-CHO��D�в���ȩ������������E��J��һ�������·�����Ϣii�����ȷ�Ӧ����KΪ �������Ϣiii�������صķ���ʽ����֪�����صĽṹ��ʽΪ��
�������Ϣiii�������صķ���ʽ����֪�����صĽṹ��ʽΪ�� ��
��| Cu |
| �� |
| Cu |
| �� |
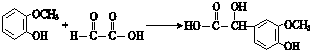 ��
��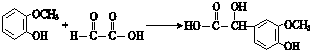 ��
��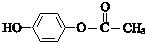 �ȣ��ʴ�Ϊ��
�ȣ��ʴ�Ϊ�� ��
�� ��
�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Br2 |
| Cu/O2 |
| �� |

 ��ϵͳ����Ϊ
��ϵͳ����Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��v��CO��=1.5 mol?L-1?min-1 |
| B��v��NO2��=0.7 mol?L-1?min-1 |
| C��v��N2��=0.4 mol?L-1?min-1 |
| D��v��CO2��=1.1 mol?L-1?min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
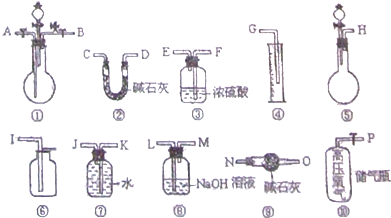
| װ������ | A | B | C | D |
| ������� | �٢ڢۢ� | �ܢݢߢ� | �٢ڢۢ�� | �ڢܢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | ����Һ��� ��mL�� | ����KMnO4�����mL�� | |
| �ζ�ǰ������mL�� | �ζ��������mL�� | ||
| 1 | 20.00 | 0.10 | 16.58 |
| 2 | 20.00 | 0.00 | 15.98 |
| 3 | 20.00 | 0.10 | 16.12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A���˷�Ӧ��ƽ�ⳣ��K=
| ||
| B���ı������÷�Ӧ��ƽ�ⳣ��Kһ������ | ||
| C���ı�ѹǿ�����������ƽ�ⳣ������֮�仯 | ||
| D��ƽ��ʱ����A��B��Ũ�ȣ�ƽ�ⳣ�����С |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com