
2012��3��22���ǵڶ�ʮ�조����ˮ�ա�������ˮ��Դ����������!
(1)C102��C12(��ԭ���ﶼΪClһ)�������г��õ��������������ĵ����ʵ�������������ʱ��C102������Ч����C12�� ����
(2)����ˮ�����ø�������(Na2Fe04��ǿ������)����ˮ�ʡ�����������������ɱ������ͬʱ����ˮ���õ�ԭ���� ��
(3)ij��ɫ��ˮ�п��ܺ���Fe3+��A13+��Mg2+��Na+��NO3-��CO32һ��SO42-�����еļ��֣�Ϊ������ɷ֣��ֱ�ȡ��ˮ��Ʒ100 mL������������ʵ�飬��������й�������ͼ��ʾ��
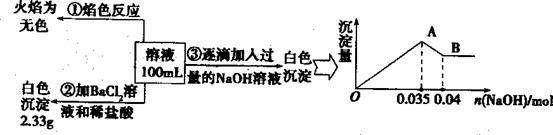
�������ͼ�ش��������⣺
��ʵ����������1��0 mol��l��NaOH��Һ80 ml�������������˲�������������ƽ����Ͳ��ҩ�ס��ձ�����ͷ�ιܣ���ȱ�ٵ�����Ϊ
��ʵ����г�������A��B��������������Ӧ�����ӷ���ʽΪ ��
����ȷ��NO3-�Ƿ����? (����ڡ��������ڡ���ȷ����)�������ڣ��Լ��� c(NO3-) (�������ڣ����ʲ�������)��

Al��OH��3 +OH-=AlO2-+2H2O Mg2++2OH-=Fe��OH��2��
n��Al3+�� 0.005mol n��Fe2+�� 0.035-3n��Al3+��
����n��Al3+��=0.005mol��n��Mg2+��=0.01mol ������Һ��Mg2+��Al3+�����������SO42-��������ɲ���ȣ���˴���NO3-����NO3-���ʵ���Ϊnmol�����ݵ���غ�ã�3n��Al3+��+2n��Mg2+��=2n��SO42-��+n��NO3-������n��NO3-��=0.015mol������c��NO3-���T0.015/0.1=0.15mol/L���ʴ�Ϊ�����ڣ�0.15mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ���ǣ� ��
A����ij����Һ�м���ŨNaOH��Һ�����Ⱥ������������ʹʪ��ĺ�ɫʯ����ֽ��������ԭ��Һһ���������Һ
B��Ũ�����е�HNO3�����ֽ⣬����ʱ��ʵ���ҿ�����Ũ����ʻ�ɫ
C����ij��Һ�м��������ữ��BaCl2��Һ��������ɰ�ɫ��������ԭ��Һ��һ��
��SO42—
D����ȥ����CO2�л��е�����SO2���ɽ������������ͨ��ʢ������KMnO4��Һ��Ũ�����ϴ��ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijͬѧģ�ҵ���۵���ȷ�������������ˮ��ԭ�������������о���
| װ�ã����������ã��Լ������ӣ� | ���� | ���� |
|
| ��Һ©����������μ���Ũ��ˮ | ����C��������ɫ��dz �����Ժ�C�г��ְ��̲������� |
Ũ��ˮ�ֽ�����ư�����д��A�з�Ӧ�Ļ�ѧ����ʽ�� ��
�Ǵ�ƽ���ƶ��ĽǶȷ���NaOH�����ڰ�ˮ�ֽ��е�����
��
��2������C�з����ķ�ӦΪ��2NH3(g)��3Cl2(g)�� N2(g)��6HCl(g) H= ��456 kJ��mol-1
��֪��
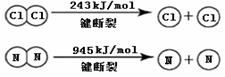
��NH3�ĵ���ʽ�� ��
�ڶϿ�1mol H��N����Ͽ�1molH��Cl�������������ԼΪ ��
��3�������в������̵Ļ�ѧ����ʽ�� ��
��4��Ϊ�������ɰ��̣���ѧ���������ͼװ�������Cl2��NH3�ķ�Ӧ��
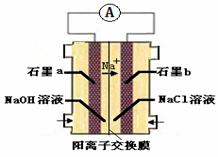
����װ����ʵ�����Ŀ�꣬���ʯīb�缫�Ϸ������� ��Ӧ�����������ԭ����
��д��ʯīa�缫�ĵ缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���в���ȷ���� ( )
A������з�̪��ˮ�м������Na202��ĩ������Һ����ɫ����ֱ���ɫ
B�������Na202��ĩ����֬���ϵμӼ���ˮ����֬����ȼ��������˵��Na202��H20��Ӧ��һ�����ȷ�Ӧ������������
C��Na202��H20��Ӧ��һ��������ԭ��Ӧ��Na202���������������ǻ�ԭ��
D��Na202��H20��Ӧ��һ���û���Ӧ���е���02����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ij���º��ݵ��ܱ������ڷ�����Ӧ��2A(g)��B(g)  C(g)����H<0����ʼ����2mol A��2mol B�����ﵽƽ��״̬������˵����ȷ����( )
C(g)����H<0����ʼ����2mol A��2mol B�����ﵽƽ��״̬������˵����ȷ����( )
A���ٳ���2mol A��ƽ�����ƣ�A��ת��������
B����������¶ȣ�C�������������
C���������ѹǿ����ѧƽ��һ��������Ӧ�����ƶ���B�����������С
D���ٳ���1mol C��C�����ʵ���Ũ�Ƚ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ʵ����ѡ���װ�û��������г�װ������ȥ����ȷ����(����)
| A | B | C | D | |
| ʵ �� | ���뱥��Na2CO3��Һ��CH3COOC2H5 | ��ȥ���еı��ӣ��ȼ�������ˮ | ��KI��I2�Ĺ��� ������л���I2 | ����100 mL 0.1000 Mol/L K2Cr2O7��Һ |
| װ �� �� �� �� |
|
|
|
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ����������ͨ��30 mLŨ��Ϊ10.00 mol/L����������Ũ��Һ�У���������ʱ�����Һ���γ�NaCl��NaClO��NaClO3������ϵ�������ж���ȷ���� (����)
A����NaOH��Ӧ������һ��Ϊ0.3 mol
B��n(Na��)��n(Cl��)����Ϊ7��3
C������Ӧ��ת�Ƶĵ���Ϊn mol����0.15��n��0.25
D��n(NaCl)��n(NaClO)��n(NaClO3)����Ϊ11��2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ұ�������ķ�Ӧԭ�����������
A��2NaCl (����)  2Na+Cl2 �� B��MgO + H2
2Na+Cl2 �� B��MgO + H2  Mg + H2O
Mg + H2O
C��Fe3O4 + 4CO  3Fe + 4CO2 D��Fe+CuSO4=FeSO4+Cu
3Fe + 4CO2 D��Fe+CuSO4=FeSO4+Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������У���Ϊͬ���칹����ǣ� ��
A�����ۺ������� B�����Ǻ���ά��
C�����ۺ���ά�� D�����Ǻ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com