
��ijһ�ݻ�Ϊ2 L���ܱ������ڣ�����2 mol��CO��2 mol��H2O�����¼��ȣ��������·�Ӧ��CO(g) +H2O(g) CO2(g) + H2(g)��1molCO��ȫ��Ӧ����a kJ����Ӧ�ﵽƽ����n(CO2)=0.8mol����˵����ȷ����( )
A���жϸ÷�Ӧ�ﵽƽ���������CO��H2O��CO2��H2��Ũ�ȶ����
B����Ӧ�ų�������Ϊ0.4a kJ
C��ƽ��ʱH2O ��ת����Ϊ40%
D������������Է�Ӧ�ӿ죬���ȸ���
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A.��Ӧ�ų�������Ϊ0.
B.��ƽ��ʱH2O��CO��ת�������
C.�������������ѹ��Ϊ
D.�жϸ÷�Ӧ�ﵽƽ���������CO��H2O��CO2��H2��Ũ�ȶ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

(��)
H2(g)+I2(g)![]() 2HI(g)������ӦΪ���ȷ�Ӧ��
2HI(g)������ӦΪ���ȷ�Ӧ��
�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=![]() ����Ӧ�����ʵ�Ũ����ʱ��仯�����ͼ(��)��
����Ӧ�����ʵ�Ũ����ʱ��仯�����ͼ(��)��
��1������ͼ(��)���ݣ���Ӧ��ʼ���ﵽƽ��ʱ��ƽ������v��HI��Ϊ_______________��
��2����Ӧ�ﵽƽ���8����ʱ��
���������¶ȣ���ѧƽ�ⳣ��K______________����������С�䣩
HIŨ�ȵı仯��ȷ����______________������ͼ(��)��a��c�ı������
��������I2��H2Ũ�ȵı仯��ȷ����_______________������ͼ(��)��d��f�ı������
��3����Ӧ�ﵽƽ���8����ʱ�������������ݻ�����һ��������ͼ(��)�л���8���Ӻ�HIŨ�ȵı仯�����

(��)
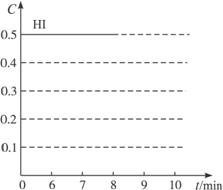
(��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ijһ�ݻ�Ϊ2 L���ܱ������ڣ�����0.8 mol��H2��0.6 mol��I2����һ���������·������·�Ӧ��
H2��g��+I2(g)![]() 2HI(g)+Q(Q>0)
2HI(g)+Q(Q>0)
��Ӧ�и����ʵ�Ũ����ʱ��仯�����ͼ1��

ͼ1
��1������ͼ1���ݣ���Ӧ��ʼ���ﵽƽ��ʱ��ƽ������v(HI)Ϊ______________________��
��2����Ӧ�ﵽƽ���8����ʱ��
���������¶ȣ���ѧƽ�ⳣ��K________________����д��������С�����䡱����HIŨ�ȵı仯��ȷ����_________________����ͼ2��a��c�ı�Żش𣩡�

ͼ2
��������I2��H2Ũ�ȵı仯��ȷ����________________����ͼ2��d��f�ı�Żش𣩡�
��3����Ӧ�ﵽƽ���8����ʱ�������������ݻ�����һ��������ͼ3�л���8���Ӻ�HIŨ�ȵı仯�����

ͼ3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���½�ũ��ʦ���и߶���ѧ�ڵ�һ�νο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����֪��һ����������CO(g)��H2O(g)
 CO2(g)��H2(g)����ijһ�ݻ�Ϊ2 L���ܱ������У�����0.2 mol��CO��0.2 mol��H2O���ڴ������ڵ������£����¼��ȣ��������·�Ӧ��CO(g)��H2O(g)
CO2(g)��H2(g)����ijһ�ݻ�Ϊ2 L���ܱ������У�����0.2 mol��CO��0.2 mol��H2O���ڴ������ڵ������£����¼��ȣ��������·�Ӧ��CO(g)��H2O(g)  CO2(g)��H2(g)����H��a kJ/mol����Ӧ��ƽ����c(CO)��c(CO2)��3��2������˵����ȷ����
CO2(g)��H2(g)����H��a kJ/mol����Ӧ��ƽ����c(CO)��c(CO2)��3��2������˵����ȷ����
A����Ӧ�ų�������Ϊ0.04a KJ
B��ƽ��ʱH2O��ת����Ϊ40%
C���������������ѹ��Ϊ1 L�������ڸ÷�Ӧƽ�������ƶ�
D���жϸ÷�Ӧ�ﵽƽ���������CO��H2O��CO2��H2��Ũ�ȶ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��ӱ�ʡ��һ�ڶ�ѧ�����п��Ի�ѧ���������� ���ͣ�ѡ����
��ijһ�ݻ�Ϊ2 L���ܱ������ڣ�����2 mol��CO��2 mol��H2O�����¼��ȣ��������·�Ӧ��CO(g) +H2O(g) CO2(g) + H2(g)��1molCO��ȫ��Ӧ����a kJ����Ӧ�ﵽƽ����n(CO2)=
0.8mol����˵����ȷ����(
)
CO2(g) + H2(g)��1molCO��ȫ��Ӧ����a kJ����Ӧ�ﵽƽ����n(CO2)=
0.8mol����˵����ȷ����(
)
A���жϸ÷�Ӧ�ﵽƽ���������CO��H2O��CO2��H2��Ũ�ȶ����
B����Ӧ�ų�������Ϊ0.4a kJ
C��ƽ��ʱH2O ��ת����Ϊ40%
D������������Է�Ӧ�ӿ죬���ȸ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com