
【题目】已知某纯碱试样中含有 NaCl 杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
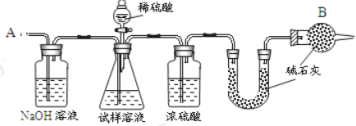
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性;
②将 a g 试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
③称量盛有碱石灰的 U 形管的质量,得到 b g;
④从分液漏斗滴入 6 molL-1的硫酸,直到不再产生气体时为止;
⑤从导管 A 处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的 U 型管的质量,得到 c g;
⑦重复步骤⑤和⑥的操作,直到 U 型管的质量基本不变,为 d g;
请填空和回答问题:
(1)第一个洗气瓶中氢氧化钠溶液的作用是____________________
(2)装置中干燥管 B 的作用是_______________________________
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果_________(填偏高、偏低或不变)。
(4)步骤⑤的目的是_______________________________________
(5)步骤⑦的目的是_________________________________________
(6)该试样中纯碱的质量分数的计算式为________________________。
【答案】吸收空气中的CO2 防止空气中的二氧化碳和水气进入U型管中 偏高 把反应产生的二氧化碳全部导入U型管中 判断反应产生的二氧化碳是否全部排出,并被U型管中的碱石灰吸收 ![]()
【解析】
实验原理是通过准确测定和酸反应生成的二氧化碳气体的量,计算碳酸钠的量;盐酸的挥发性,空气中含有二氧化碳和水蒸气都会对实验产生干扰,据此回答。
(1)空气中含有二氧化碳,氢氧化钠溶液吸收二氧化碳,防止空气中的二氧化碳气体进入U型管中的碱石灰,干扰实验;
(2)U型管中的碱石灰是为了吸收反应生成的二氧化碳,但空气中也存在二氧化碳,干燥管B的作用就是防止空气中的二氧化碳和水分进入U型管,对结果产生误差。
(3)由于盐酸具有挥发性,也会随着二氧化碳进入U型管,被误认为是二氧化碳,所以二氧化碳的质量偏大,算出的碳酸钠的质量也会偏大的,所以结果会偏大。
(4)由于反应结束后锥形瓶中存留有二氧化碳,鼓入一定量的空气就是将残留的二氧化碳完全排入U型管;步骤⑤的目的是把反应产生的二氧化碳全部导入U型管中;
(5)U型管的质量基本不变,说明二氧化碳已经被全部排到U型管中;步骤⑦的目的是判断反应产生的CO2是否全部排出,并被U型管中的碱石灰吸收;
(6)设需要碳酸钠的质量为X,则:
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 44
X d-b
列比例式:![]()
解得X=![]() ;
;
所以试样中纯碱的质量分数的计算式为![]()
![]() ;
;


科目:高中化学 来源: 题型:
【题目】(1)SO2 的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的 SO2。已知吸收过程中相关反应的热化学方程式如下:
①SO2(g)+NH3·H2O(aq)=NH4HSO3(aq) ΔH1=a kJ/mol;
②NH3·H2O(aq)+ NH4HSO3(aq)=(NH4)2SO3(ag)+H2O(l) ΔH2=b kJ/mol;
③2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) ΔH3=c kJ/mol。
则反应 2SO2(g)+4NH3·H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的 ΔH=____kJ/mol。
(2)SO2是形成酸雨的主要污染物,燃煤脱硫原理为 2CaO(s)+2SO2(g)+O2(g)2CaSO4(s)。向 10L 恒温恒容密闭容器中加入 3mol CaO,并通入 2mol SO2 和 lmol O2 发生上述反应,2min时达平衡,此时 CaSO4 为1.8mol。02min 内,用 SO2 表示的该反应的速率v(SO2)=____,其他条件保持不变,若上述反应在恒压条件下进行,达到平衡时 SO2 的转化率____(填“增大”、“减小”或“不变”)。
(3)NO 的排放主要来自于汽车尾气,净化原理为:2NO(g)+2CO(g)N2(g)+2CO2(g) ΔH=746.8kJ/mol。实验测得,v正=k正·c2(NO)·c2(CO),v 逆=k逆·c(N2)·c2(CO2)(k 正、k 逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数____(填“>”“<”或“=”)k逆增大的倍数。
②若在 1L 的密闭容器中充入 1molCO 和 1mol NO,在一定温度下达到平衡时,CO 的转化率为 40%,则k正︰k逆=____。
(4)以连二硫酸根(S2O42-)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
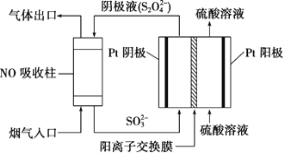
①阴极区的电极反应式为____。
②NO 吸收转化后的主要产物为 NH4+,若通电时电路中转移了 0.3mol e-,则此通电过程中理论上吸收的 NO 在标准状况下的体积为____mL。
(5)欲用 5L Na2CO3 溶液将 23.3g BaSO4 固体全都转化为 BaCO3,则所用的 Na2CO3 溶液的物质的量浓度至少为____。[已知:常温下K(BaSO4)=1×107、K(BaCO3)=2.5×106]。(忽略溶液体积的变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度不是1molL-1的是( )
A.将10g NaOH固体溶解在水中配成250mL溶液
B.将80g SO3溶于水配成1L溶液
C.将58.5gNaCl固体加入1L水后所得的溶液
D.标准状况下,将22.4L HCl气体溶于水配成1L溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物吗替麦考酚酯有强大的抑制淋巴细胞增殖的作用,可通过如下反应制得:
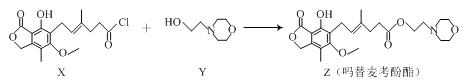 +HCl
+HCl
下列叙述正确的是
A. 用溴水可鉴别化合物X和ZB. 化合物Y的分子式为C6H14NO2
C. 化合物Z中含有手性碳原子D. 1mol化合物Z可以与3mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若气态烃A的相对分子质量为26,根据下列转化关系推断:
A![]() B
B![]() C;A
C;A![]() D
D![]() E。
E。
(1)写出A~E的结构简式:
A_____B________C_________D_________E___________
(2)写出下列反应的化学方程式:
B ![]() C:_________。
C:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 4gNaOH固体所含电子总数为2NA
B. 22.4LC2H6所含化学键总数为7NA
C. 6gSiO2所含分子数为0.1NA,化学键总数为0.4NA
D. 0.1mol·L-1NH4Cl溶液中,![]() 与Cl-数之和小于0.2NA
与Cl-数之和小于0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学小组为探究![]() 在酸性
在酸性![]() 溶液中的反应,利用如图装置进行实验:
溶液中的反应,利用如图装置进行实验:
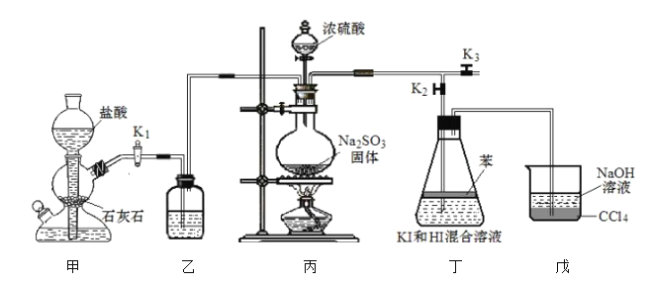
I.排出装置内的空气。减缓![]() 的流速,向丁装置中通入
的流速,向丁装置中通入![]() 和
和![]() 的混合气体。
的混合气体。
Ⅱ.一段时间后,溶液变黄并出现浑浊。摇动锥形瓶、静置,苯与溶液边缘呈紫红色。
Ⅲ.持续向丁装置中通入![]() 和
和![]() 混合气体,溶液变为无色。
混合气体,溶液变为无色。
Ⅳ.再静置一段时间,取锥形瓶中水溶液,滴加![]() 溶液,产生白色沉淀。
溶液,产生白色沉淀。
回答下列问题:
(1)苯的作用为__________。排出装置内空气的具体操作为_________。
(2)向装置丁中缓慢通入![]() 的作用是__________。
的作用是__________。
(3)步骤Ⅱ反应的离子方程式为__________;步骤Ⅲ反应的离子方程式为______________。
(4)实验的总反应为_________,![]() 和
和![]() 在反应中的作用为___________。
在反应中的作用为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。下列说法中正确的是( )
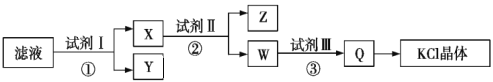
A.初始滤液显酸性
B.试剂Ⅰ为Ba(NO3)2溶液
C.步骤②中加入试剂Ⅱ的目的是除去Ba2+
D.图示步骤中的2次过滤操作不可以合并
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com