
【题目】下列热化学方程式正确的是( )
A. 甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)==CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 500 ℃、30 MPa 下,将0.1 mol N2 和 0.3 mol H2 置于密闭容器中充分反应生成NH3(g),放热3.86 kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. 已知1 g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05 kJ的热量,肼和过氧化氢反应的热化学方程式为:N2H4(l)+2H2O2(l)===N2(g)+4H2O(g) ΔH=-641.6 kJ·mol-1
D. CO的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g) △H=+283.0kJ/mol
【答案】C
【解析】A.燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ/mol中生成水是液体,故A错误;B.合成氨的反应为可逆反应,0.5molN2和1.5mol H2置于密闭的容器中充分反应生成NH3(g)的物质的量小于1mol,所以生成1mol氨气放出的热量大于放热19.3kJ,故B错误;C.1g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05kJ的热量,则1mol肼反应放出的热量为32×20.05=641.60(kJ)所以肼和过氧化氢反应的热化学方程式为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.6 kJmol-1,故C正确;D.因CO(g)的燃烧热是283.0KJ.mol-1,则2CO(g)+O2(g)=2CO2(g)反应的△H=-2×283.0KJ.mol-1,则2CO2(g)=2CO(g)+O2(g)反应的△H=2×283.0KJ.mol-1,故D错误;答案为C。


科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 二氧化硅用于制备太阳能
B. 二氧化硅是生产光导纤维的主要材料
C. 从海水中提取物质不一定必须通过化学反应才能实现
D. 氢氟酸不能保存在玻璃瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用四氯化碳萃取碘的饱和水溶液中的碘,下列说法不正确的是( )
A.实验使用的主要仪器是分液漏斗
B.分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出
C.碘在四氯化碳中的溶解度比在水中的溶解度大
D.碘的四氯化碳溶液呈紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磺化钠在医药中用作甲状腺肿瘤防治剂、袪痰剂和利尿剂,也用作食品添加剂、感光剂等。工业上用水合肼(N2H4·H2O)还原法制取碘化钠固体,其制备流程如图所示:
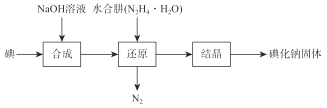
己知:N2H4·H2O在100℃以上分解。
(1)在合成NaI的过程中,可能混有的物质是_______,生产过程中要适当补充NaOH,目的是________。
(2)在还原过程中,为了防止水合肼(N2H4·H2O)高温分解,反应温度控制在60~70℃,温度也不能过低,其原因是___________。工业上也可以用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因是_____________________。
(3)请设计一个简单的实验来检验还原液中是否含有IO3-:__________________。(可供选择的试剂:稀硫酸、淀粉溶液、FeCl3溶液)
(4)测定产品中NaI含量的实验步骤如下:
a.称取4.000 g样品并溶解,在250 mL容量瓶中定容;
b.量取25.00 mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入A溶液作指示剂;
c.用0.1000mol·L-1的Na2S2O3溶液滴定至终点(发生反应方程式为:2Na2S2O3+I2=Na2S4O6+2NaI),重复测定3次,所得的相关数据如表所示:
测定序号 | 待测体积/ml | 盛装标准滴定管的起点读数/ml | 盛装标准滴定管的终点读数/ml |
1 | 25.00 | 0.06 | 24.04 |
2 | 25.00 | 0.02 | 24.02 |
3 | 25.00 | 0.12 | 24.14 |
①在滴定过程中,Na2S2O3溶液应放___________(填仪器)中;加入的A物质为____________(填名称)。
②滴定终点观察到的现象为_______________________。
③该样品中NaI的含量为_______________________。
④若用上述方法测得NaI的含量偏低(忽略测定过程中的误差),则可能的原因是_________________。
(5)碘化钠固体的保存方法是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列一卤代烷,不能发生消去反应的是 ( )
A. CH3CH2ClB. (CH3)2CHClC. (CH3)3CClD. (CH3)3CCH2Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 由极性键结合而成的分子一定是极性分子
B. 非极性键只存在于双原子单质分子里
C. 非极性分子中,一定含有非极性键
D. 一般情况下,极性分子易溶于极性溶剂,非极性分子易溶于非极性溶剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为 11℃,可用于处理含硫废水。某小组在实验室中探究 ClO2 与 Na2S 的反应。回答下列问题:
(1)ClO2 的制备
已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4
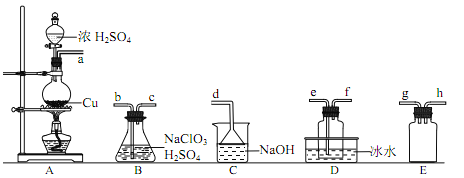
①装置 A 中反应的化学方程式为____________。
②欲收集干燥的 ClO2,选择上图中的装置,其连接顺序为 a→________________(按气流方向,用小写字母表示)
③装置 D 的作用是__________________。
(2)ClO2 与 Na2S 的反应
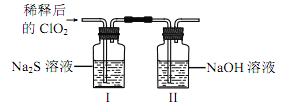
将上述收集到的 ClO2 用 N2 稀释以增强其稳定性,并将适量的稀释后的 ClO2 通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究 I 中反应的产物。
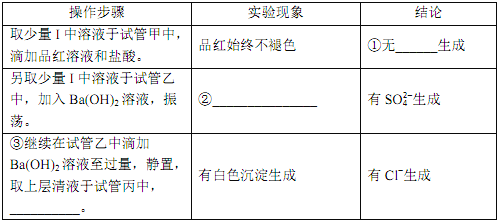
①___________。②___________。③___________。
④ClO2 与 Na2S 反应的离子方程式为____________。用于处理含硫废水时,ClO2 相对于Cl2 的优点是____________(任写一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,可行的是( )
A.用食醋除去热水瓶中的水垢
B.用米汤检验加碘盐中的碘酸钾(KIO3)
C.向Al2(SO4)3溶液中加过量NaOH溶液,制Al(OH)3
D.向稀H2SO4催化水解后的麦芽糖溶液中直接加入新制Cu (OH)2悬浊液,检验水解产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com