
| A. | 重金属盐类能使蛋自质凝结.所以误食重金属盐类能使人中毒 | |
| B. | 在蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,虽再加水,也不溶解 | |
| C. | 人工合成具有生命活力的蛋白质--结晶牛胰岛素是我国科学家在1965年首次合成 | |
| D. | 浓硝酸溅在皮肤上能使皮肤呈现黄色,是由于浓硝酸和蛋白质发生了颜色反应 |
分析 A.重金属盐能使蛋白质发生变性;
B.蛋白质溶液中加入饱和硫酸铵溶液,发生盐析,为可逆过程;
C.结晶牛胰岛素为中国首次合成蛋白质;
D.含苯环的蛋白质,遇浓硝酸发生颜色反应,变为黄色.
解答 解:A.重金属盐能使蛋白质发生变性,则重金属盐类能使蛋自质凝结,误食重金属盐类能使人中毒,故A正确;
B.蛋白质溶液中加入饱和硫酸铵溶液,发生盐析,为可逆过程,则蛋白质析出,再加水,又溶解,故B错误;
C.结晶牛胰岛素是我国科学家在1965年首次合成具有生命活力的蛋白质,故C正确;
D.含苯环的蛋白质,遇浓硝酸发生颜色反应,变为黄色,则浓硝酸溅在皮肤上能使皮肤呈现黄色,是由于浓硝酸和蛋白质发生了颜色反应,故D正确;
故选B.
点评 本题考查蛋白质的性质,为高频考点,把握蛋白质的变性、盐析、颜色反应为解答的关键,侧重分析与应用能力的考查,注意盐析为可逆过程,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 加水 | B. | 增加同浓度FeSO4的用量 | ||
| C. | 加压 | D. | 加入少量KMnO4晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,则原有机物一定是( )
,则原有机物一定是( )| A. | 1,3-丁二烯 | B. | 2-甲基-1,3-丁二烯 | ||
| C. | 2-丁炔 | D. | 1,4-二氯-2-甲基-2-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
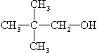 ;
;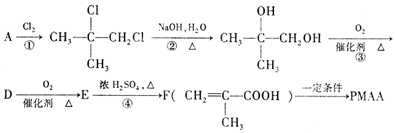

 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O
+2H2O $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$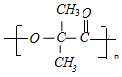 +nH2O.
+nH2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
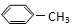 分子结构的下列叙述中,正确的是( )
分子结构的下列叙述中,正确的是( )| A. | 七个碳原子可能不在同一平面上 | B. | 具有单键和双键两种键 | ||
| C. | 八个氢原子不可能都在同一平面上 | D. | 最多可能有5个C原子在一条直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com