
����Ŀ����ϩ��Ϊԭ�ϣ��ϳ�ijЩ�߾����·����ͼ��

��֪������![]() ����д��
����д��![]() R����ȡ�������⣩
R����ȡ�������⣩
��������
����F����NaHCO3��Ӧ����CO2������������⣺
��1��CH3CH=CHCH3��������______��Br2��CCl4��Һ��______ɫ��
��2��X��Y�ķ�Ӧ����Ϊ��______��D��E�ķ�Ӧ����Ϊ��______��
��3��H�Ľṹ��ʽ��______��
��4��д�����л�ѧ����ʽ��
A��B______��
Z��W______��
��5���������������߾���H�IJ��ʲ������Ԥ�ڣ����ʲ��ߵ�ԭ�������______��
���𰸡�2����ϩ �Ⱥ� ȡ����Ӧ ��ȥ��Ӧ 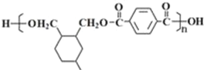
![]()
![]() �ϳɲ�����ࡢ�л���Ӧ�Ƚϸ���
�ϳɲ�����ࡢ�л���Ӧ�Ƚϸ���
��������
2-��ϩ�������ڹ��������·���ȡ����Ӧ����X��X�����������ӳɷ�Ӧ����A��A���������ƵĴ���Һ������ȥ��Ӧ����B��B����ϩ��Ӧ���ɻ���ϩ����������Ϣ֪��B��CH2=CH-CH=CH2����AΪClCH2CH2CH2CH2Cl��XΪClCH2CH=CHCH2Cl������ϩ���巢���ӳɷ�Ӧ����DΪ![]() ��D���������ƴ���Һ�����������·�����ȥ��Ӧ����EΪ
��D���������ƴ���Һ�����������·�����ȥ��Ӧ����EΪ![]() ��E�����Ӿ۷�Ӧ�õ�
��E�����Ӿ۷�Ӧ�õ�![]() ��X����ˮ�ⷴӦ����YΪHOCH2CH=CHCH2OH��Y����������Ӧ����ZΪHOCCH=CHCHO����Ϊ����Z�ͼ�Ӧ����W��W�����������ӳɷ�Ӧ����
��X����ˮ�ⷴӦ����YΪHOCH2CH=CHCH2OH��Y����������Ӧ����ZΪHOCCH=CHCHO����Ϊ����Z�ͼ�Ӧ����W��W�����������ӳɷ�Ӧ����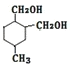 ����������Ϣ֪��Z�ͼ����ӳɷ�Ӧ�����ԼĽṹ��ʽΪ��
����������Ϣ֪��Z�ͼ����ӳɷ�Ӧ�����ԼĽṹ��ʽΪ��![]() ��W�Ľṹ��ʽΪ��
��W�Ľṹ��ʽΪ��![]() ��1��4-���ױ������Ը��������������FΪ
��1��4-���ױ������Ը��������������FΪ![]() ��
��![]() ��
�� �������۷�Ӧ��Ӧ����H����H�Ľṹ��ʽΪ��
�������۷�Ӧ��Ӧ����H����H�Ľṹ��ʽΪ��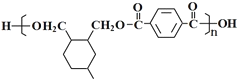 ���ݴ˽��
���ݴ˽��
��1��CH3CH=CHCH3�������ǣ�2��ϩ��Br2��CCl4��Һ�ʳȺ�ɫ��
��2��X��Y��ClCH2CH=CHCH2Cl����ˮ�ⷴӦ����YΪHOCH2CH=CHCH2OH������ȡ����Ӧ��D��E��![]() ���������ƴ���Һ�����������·�����ȥ��Ӧ����
���������ƴ���Һ�����������·�����ȥ��Ӧ����![]() ���ʴ�Ϊ��ȡ����Ӧ����ȥ��Ӧ��
���ʴ�Ϊ��ȡ����Ӧ����ȥ��Ӧ��
��3��H�Ľṹ��ʽ�ǣ�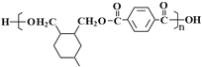 ��
��
��4��A��B�ķ�Ӧ����ʽΪ��![]() ��Z��W�ķ�Ӧ����ʽΪ��
��Z��W�ķ�Ӧ����ʽΪ��![]() ��
��
��5���������������߾���H�IJ��ʲ������Ԥ�ڣ����ʲ��ߵ�ԭ������ǣ��ϳɲ�����ࡢ�л���Ӧ�Ƚϸ��ӣ��ʴ�Ϊ���ϳɲ�����ࡢ�л���Ӧ�Ƚϸ��ӡ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ����˹��̵�����Ҫ��;������Ӧ���Ȼ�ѧ����ʽ���£�N2(g)+3H2(g)![]() 2NH3(g) ��H=-92.4kJ��mol-1��
2NH3(g) ��H=-92.4kJ��mol-1��
��1����ҵ����������ߺϳɰ����ʵ�������___��
A.���� B.���� C.��ѹ D.��ѹ E.����
��2�����ںϳɰ���˵������ȷ����__��
A.�ϳɰ���Ӧ����H����S��С����
B.������773K�·�Ӧ��Ŀ���Ǽӿ췴Ӧ���ʺ����ƽ��ת����
C.��NH3Һ������ȥ�����ڷ�Ӧ������ߺ�ƽ�������ƶ�
D.ԭ�����뾭�������������Է�ֹ�����ж����¹ʷ���
��3����N2��H2�ij�ʼͶ�����ֱ�Ϊ0.1mol��0.3mol���ں��������з�Ӧ��ƽ��������а����������(��)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
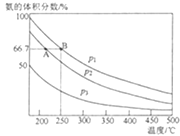
�ٱȽ�p2��p3�Ĵ�С��p2__p3������������������������������ԭ����__��
�ڱȽ�ƽ��ʱA��B���Ӧ�Ļ�ѧ��Ӧ���ʣ�VA(N2)__VB(N2)����������������������������
������ʼѹǿΪ1��108Pa����ƽ��ʱB���ѹǿΪ___Pa��
��4����ѧ�ҷ��֣���H2O��N2Ϊԭ�ϣ�����NaOH-KOHΪ����ʣ�����Fe2O3����������250��ͳ�ѹ�¿�ʵ�ֵ绯ѧ�ϳɰ��������������ı仯�ɰ��������С���֪��һ���ķ�ӦΪ��Fe2O3+6e-+3H2O=2Fe+6OH-����ڶ����ķ�Ӧ����ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
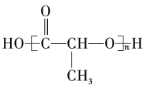
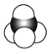
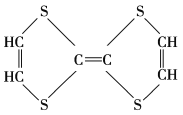
����Ŀ���л���ı�ʾ�������ֶ������������ò�ͬ������ʾ�ļ����л��
�� ��
��![]() ��
�� ��
��
�� ��
��
��
��
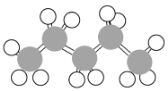
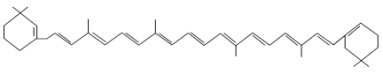
��1��������ʾ���������ڽṹ��ʽ��Ϊ______������ţ���ͬ�������ڽṹʽ��Ϊ______�����ڼ���ʽ��Ϊ______�����ڱ���ģ�͵�Ϊ______���������ģ�͵�Ϊ______��
��2��д���������������ŵĵ���ʽ��______��______��
��3���ٵķ���ʽΪ______�����ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȵ�Na2O2��NaHCO3��������һ�ݼ��������������ַ�Ӧ��ų�2.24L����״���������壻����Щ����ͨ����һ�ݻ������ʹ���ַ�Ӧ�����������Ϊ2.016L����״��������ԭ�������Na2O2��NaHCO3�����ʵ���֮��Ϊ
A.8��1B.2��1C.3��2D.2��9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨʵ���ҳ��ڴ�ŵ�Na2SO3����Ĵ��ȣ�ȷ��ȡW g������Ʒ�����250 mL��Һ���������������ʵ�鷽����
������ȡ25.00 mL������Һ�������������ù��������ữ��BaCl2��Һ�����ˡ�ϴ�Ӻ���������Ƶó���������Ϊm1 g��
������ȡ25.00 mL������Һ����������������ữ��Ba(NO3)2��Һ�����ˡ�ϴ�Ӻ�����������أ�������Ϊm2 g��
(1)����250 mL Na2SO3��Һʱ�������õ���ʵ�������У��ձ�������������ͷ�ιܡ�ҩ�ס�________________��________��
(2)д��Na2SO3�����������ʵĻ�ѧ����ʽ_____________��
(3)�������������������ữ��BaCl2��Һ��Ŀ����__________________________��
�ڹ���ǰ����Ҫ�����Ƿ������ȫ���������______________��
(4)�������У�����Һ���ǣ������²ⶨ���________(�ƫ�ߡ���ƫ�͡�)��
(5)��������ȷ����m1________m2(�����������������)��ԭ����_______________��
(6)ȡ25.00 mL������Һ��������KMnO4��Һ�ζ��ķ����ⶨNa2SO3�Ĵ��ȡ���֪���������£�KMnO4ͨ������ԭΪMn2������Na2SO3����Ĵ��ȿɱ�ʾΪ_____________(ע������ʽ�����õ��йط��ŵĺ���͵�λ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ϡ�����һԪ��BOH��Һ��������(���Ի�Ϻ���Һ������仯)��ʵ���������±���

��ش�
(1)HCl��Һ��BOH��Һ��Ӧ�����ӷ���ʽΪ___________________��
(2)ʵ��ٷ�Ӧ�����Һ����ˮ�������c(OH-)=_________mol��L-1��ʵ��۷�Ӧ�����Һ����ˮ�������c(OH-)=_________mol��L��1
(3)x_________0.2 mol��L-1(����>����<������=����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B�����������ʽ��ͬ��7.8gA��ȫȼ�պ�������ͨ�������ʯ��ˮ�У��õ�����60g���ȿ���������KMnO4��Һ��A��B���м���Ҳ��������ˮ��Ӧ�����ǽ��м���0.5mol B��ȫȼ������22.4LCO2(��״��)��9gˮ������ͬ״���£�A��B�������ܶȱ�Ϊ3��1����ͨ�������ƶ����������Ľṹ��ʽ��__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A�����ҺpH=a��B�����ҺpH=b
��1����AΪ���ᣬBΪ������������a+b=14�����ߵ������ϣ���Һ��pH=____���������Ϊ1��10��Ϻ���Һ�����ԣ���a+b=____________��
��2����AΪ���ᣬBΪ�������ƣ���a=4��b=12����ôA��Һ��ˮ�������������Ũ��Ϊ__________mo1��L�Cl��B��Һ��ˮ�������������Ũ��Ϊ____________mol��L�C1��
��3����AΪ���ᣬBΪ�������ƣ���a+b=14�������ΪVA�Ĵ�������ΪVB������������Һ��Ϻ���Һ�����ԣ����������ϵVA _____________VB����Ϻ���Һ�е�����Ũ�ȹ�ϵΪc(Na+)___________c(CH3COO-)��
��4����A�Ļ�ѧʽΪHR��B�Ļ�ѧʽΪMOH����a+b=14�����ߵ������Ϻ���Һ�Լ��ԡ�������Һ�бض���һ�������ܷ���ˮ�⣬��ˮ�ⷴӦ�����ӷ���ʽΪ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaHCO3��Na2O2�Ĺ�������x g���ܱ������м�����250������ַ�Ӧ���ų����壮����Ӧ��Ĺ�������ˮ������ų�������μ������ᣬ�������壨��״�����������������֮��Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
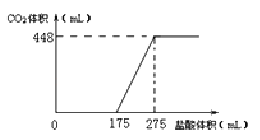
A��HCl��Ũ��0.2mol/L
B����Ӧ�����ijɷ�ΪNaOH��Na2CO3
C���ܱ��������ų�����ijɷ�ΪO2��H2O
D��x����ֵΪ6.09
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com