
����Ŀ��25��ʱ����0.1molL-1��NaOH��Һ�ֱ�ζ�20.00mLŨ�Ⱦ�Ϊ0.10molL-1��CH3COOH��Һ��HCN��Һ�����õζ�������ͼ������˵����ȷ����

A. ��Ϊ�ζ��յ㣬���ü�����ָʾ��
B. �����͵�����ʾ��Һ�У�c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
C. �����͵�����ʾ��Һ�У�c(CH3COO-)��c(CN-)
D. �����͵�����ʾ��Һ�У�c(CH3COO-)+ c(CH3COOH)��ֵ���
���𰸡�B
�����������������A���ζ��յ���ָ���ǡ����ȫ��Ӧʱ��ĵ㣬��ͼ��֪���������NaOH���㣬��û���ζ��յ㣬��A����B�����������غ�ã�c(CH3COO-)+c(CH3COOH)=c(CN-)+c(HCN)�����Ե�c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)����B��ȷ��C��������Һ�ʼ��ԣ���c(OH-)>c(H��)��˵��CN-ˮ��̶ȴ���HCN����̶ȣ���c(CN-)��c(Na��)��c(HCN)��������Һ�����ԣ���c(OH-)��c(H��)��˵��CH3COO-ˮ��̶�С��CH3COOH����̶ȣ�����c(CH3COO-)>c(Na��)>c(CH3COOH)����c(CH3COO-)>c(CN-)����C����D�����������غ��֪�������͵�����ʾ��Һ�У�n(CH3COO-)+ n(CH3COOH)��ֵ��ȣ���������Һ���������c(CH3COO-)+ c(CH3COOH)��ֵ��С����D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵķе��ɸߵ������е���
��CH3��CH2��2CH3
��CH3��CH2��3CH3
����CH3��3CH
����CH3��2CHCH2CH3��
A���ܢڢ٢�
B���ڢܢ٢�
C���ܢ٢ڢ�
D���ڢܢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����DNA�����һ�ֱ۳�ֻ��7nm���������ӣ�����������ǯ����ӻ�ԭ�ӣ���������������ϡ����з�ɢϵ�з�ɢ�ʵ���ֱ�����������Ӿ�����ͬ����������( )
A����Һ B������ C������Һ D������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�������ϸ��¶ȣ�����������ȷ����( )
A. ˮ�����ӻ����pH��С��������
B. ˮ�����ӻ����䡢pH���䡢������
C. ˮ�����ӻ����pH��С��������
D. ˮ�����ӻ���С��pH��ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С��������ϵ�֪������Һ�������廯����FeBr3�����ڵ������¿ɷ�����Ӧ�����屽���廯�⣬�˷�ӦΪ���ȷ�Ӧ�������������ͼװ����ȡ�屽�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A�С���ͼ����ȡ�屽��װ�á��Իش�
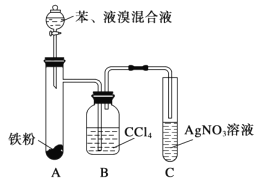
��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽ��______________________��
��2��װ��C�п�����������______________��֤��________________��
��3��װ��B������ƿ����ʢCCl4Һ�塣���û��Bװ�ö���A��Cֱ������������Ϊ�Ƿ�����__________����������������������������_____________________��
��4��ʵ����Ϻ�A�Թ��е�Һ�嵹��װ����ˮ���ձ��У��ձ�_________����������������������Ϊ�屽����˵���屽___________��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��0.1mol/L��CH3COONa��Һ��pH=a��������˵����ȷ����
A��a<7
B������Һ��ˮ�����c(OH-)=10-amol/L
C��CH3COO-ˮ��İٷ���Ϊ(10-a/0.1)��100��
D��c(CH3COOH)= (l0a-14��10-a)mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2-���������������ȡ����Ӧ���õ���һ�ȴ��ﹲ�У� ��
A. 3�� B. 4�� C. 5�� D. 6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������CO2��H2�ɷ�����Ӧ��CO2(g)+ H2(g)![]() CO (g)+H2O(g) ��H
CO (g)+H2O(g) ��H
��֪����CO��H2��ȼ���ȷֱ�Ϊ-283.0 kJmol-1 ��-285.8kJmol-1
��H2O��l��= H2O��g�� ��H=+44.0KJ��mol-1
��1��д����ʾH2ȼ���ȵ��Ȼ�ѧ����ʽ____________________��
CO2��g��+ H2��g��![]() CO��g��+ H2O��g�� ��H1=___________KJ��mol-1
CO��g��+ H2O��g�� ��H1=___________KJ��mol-1
��2�����������CO2ƽ��ת���ʵĴ�ʩ��__________��
A����ѹ B������
C������CO2Ũ�� D��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ��
��3����CO2��H2��ʼͶ�ϱ�Ϊ1:1����Ӧ��ƽ��ʱCO��ƽ�������е��������Ϊ25%����CO2��ת����Ϊ_________���÷�Ӧ��ƽ�ⳣ��Ϊ_________����CO2��H2��ʼͶ�ϱȸ�Ϊ1:2����CO2��ƽ��ת����Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼ�ϵ����ȼ�ϣ�����CO��H2��CH4�ȣ��������������Ӧ�����˷�Ӧ�Ļ�ѧ��ת��Ϊ���ܵ�װ�ã������ͨ����KOH��Һ�����й��ڼ���ȼ�ϵ�ص�˵������ȷ����
A��������ӦʽΪCH4+10OH--8e=CO32-+7H2O
B��������ӦʽΪO2+2H2O+4e=4OH-
C�����Ų��Ϸŵ磬�������Һ���Բ���
D������ȼ�ϵ�ص����������ʱȼ���ȼ�յ����������ʴ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com