
【题目】如图是某同学设计用来验证SO2性质的微型实验装置。分析实验,下列结论不正确的是( )
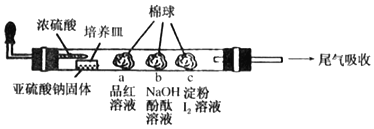
A.棉球a褪色,说明SO2具有漂白性
B.棉球b褪色,说明SO2具有氧化性
C.棉球c褪色,说明SO2具有还原性
D.可以用氨水或高锰酸钾溶液吸收尾气
科目:高中化学 来源: 题型:
【题目】某致病细菌分泌的外毒素,无色,细针状结晶,对小鼠和人体有很强的毒性,可引起流涎、呕吐、便血、痉挛等,以致死亡。该外毒素为环状肽,结构式如图所示,请据图分析回答:

(1)该化合物中含有游离的氨基_____________个,羧基________________个。
(2)该化合物是由_____________个氨基酸组成的,区别这些氨基酸的种类是依靠其结构中的_____________。
(3)组成该化合物的氨基酸有___________种,其中有_____________个氨基酸的R基相同,这个R基是_______________。
(4)该化合物称为环状__________肽化合物,含有___________个肽键。
(5)填写虚线框内结构的名称:A._________________,B.___________________。
(6)该化合物具有8个氮原子,其中_____________个位于肽键上,____________个位于R基上。
(7)该外毒素环肽在形成过程中失去了______________个水分子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)密闭容器中mA(g)+nB(g)![]() pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
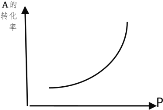
①增大压强,A的转化率___平衡向___移动,达到平衡后,混合物中C的浓度___。
②上述化学方程式中的系数m、n、p的正确关系是____。
③当降低温度时,C的浓度减小,正反应是___热反应。
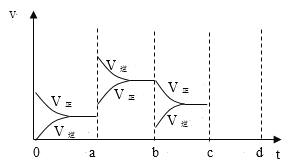
(2)如图表示在密闭容器中反应:2SO2(g)+O2(g)![]() 2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是___;b-c过程中改变的条件可能是____;若增大压强时,反应速度变化情况画在c-d处。___
2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是___;b-c过程中改变的条件可能是____;若增大压强时,反应速度变化情况画在c-d处。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电化学的叙述正确的是( )
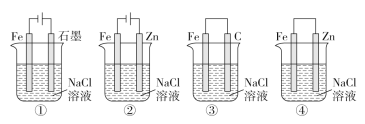
A. 图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红
B. 图②装置中Fe电极参与反应发生腐蚀
C. 图③可以模拟钢铁的吸氧腐蚀,碳棒一极的电极反应式:O2+2H2O+4e-=4OH-
D. 上述4个装置中,图①、②中Fe腐蚀速率较快,图③中Fe腐蚀速率较慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含钒石煤(含有铁、硅、铝、钙、镁等元素的氧化物)中的钒大部分是以V(III)和V(IV)形式存在,由含矾石煤提钒的一种工艺流程如图所示:

已知:铜铁试剂能与铜、铁、铝、钛等元素形成不溶于水的配合物。
回答下列问题:
(1)含矾石煤预制时加入复合添加剂对钒浸出率的影响如图所示,其中最佳复合添加剂为__,最佳添加比例为__。

(2)如图为“抽滤”实验原理装置图,"抽滤”时抽气泵的作用是__;“酸浸渣”经“水洗涤”返回“浸出”的目的是__。

(3)已知酸浸液中V2O24+被H2O2氧化成VO2+,其离子方程式为__。“净化除杂”时用铜铁试剂除去所含的Al3+、Fe3+等杂质离子而不通过调节酸浸液pH的原因是__。
(4)“沉钒”的离子反应方程式为___。
(5)“煅烧”纯净的沉钒产物过程中,固体残留率与温度变化如图所示。已知A点坐标为(260℃,85.47%)。则A点对应物质的化学式为__,B点对应的物质为V2O5,则B点坐标为___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】荣获2019年诺贝尔化学奖的吉野彰是最早开发具有商业价值的锂离子电池的日本科学家,他设计的可充电电池的工作原理示意图如图所示。该可充电电池的放电反应为LixCn+Li(1-x)CoO2=LiCoO2+nC。NA表示阿伏伽德罗常数的值。下列说法错误的是( )
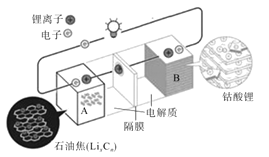
A.该电池用于电动汽车可有效减少光化学烟雾污染
B.充电时,正极反应为LiCoO2-xe-=Li(1-x)CoO2+xLi+
C.放电时,Li+由A极移向B极
D.若初始两电极质量相等,当转移2NA个电子时,两电极质量差为14g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A.次氯酸钠中氯元素的化合价:+1
B.氟原子的结构示意图:![]()
C.明矾的化学式:KAlSO412H2O
D.硫酸的电离方程式:H2SO4=H2++SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用MnO2和浓盐酸制取氯气时,有14.6 g氯化氢被氧化,所得Cl2全部用石灰水吸收,可制得漂白粉的质量是
A. 14.3 g B. 25.4 g C. 28.6 g D. 50.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物甲(![]() ,
,![]() ),性质类似卤素单质。将2.335g甲加热至完全分解,生成0.01mol液体乙和224mL(标准状况下)黄绿色的单质气体丙。请回答:
),性质类似卤素单质。将2.335g甲加热至完全分解,生成0.01mol液体乙和224mL(标准状况下)黄绿色的单质气体丙。请回答:
(1)甲加热至完全分解的化学方程式是________。
(2)乙与水反应的离子方程式是_________。
(3)下列有关化合物甲和乙的说法正确的是________。(填字母)
A.甲不能与可燃物、碱类一起储运
B.一定条件下乙能与乙烯或苯反应
C.甲分子中各原子均达到8电子稳定结构
D.粗碘中常混有乙,可直接用升华法分离提纯碘
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com