
����Ŀ��ԭ���ԭ���ķ����Ǵ��ܺ��ܼ����ľ�������ǻ�ѧ�������һ���ش��ס�
(1)����пƬ�ʹ�ͭƬ��ͼ��ʽ����100 mL��ͬŨ�ȵ�ϡ������һ��ʱ�䣬�ش��������⣺
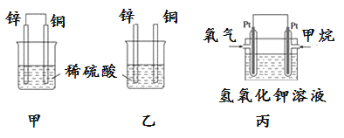
������˵����ȷ����____________��
A���ס��Ҿ�Ϊ��ѧ��ת��Ϊ���ܵ�װ�� B������ͭƬ��û�����Ա仯
C������ͭƬ�������١�����пƬ�������� D���������ձ�����Һ�� pH ������
��ͬ���������ձ��в���ͬ��������壬��Ҫ��ʱ���________��(����>����<����������)��
����д������ͼ�й���ԭ��صĸ����缫��Ӧʽ��__________________��
����������Һ��������15.75gʱ���缫��ת�Ƶ�����ĿΪ______________��
(2) ͼ��Ϊ��������ȼ�ϵ�صĹ���ʾ��ͼ���������Һ��������KOH��д�������ĵ缫��Ӧ����ʽΪ____________________________________��
���𰸡�BD < Zn��2e��=Zn2�� 0.5 NA CH4+10OH--8e-=CO32-+7H2O
��������
(1)��ͼ֪����Ϊԭ��أ��Ҳ�����ԭ��أ���������װ�����ܷ�Ӧ��Ϊп��ϡ���ᷴӦ��������п���ų��������ݴ˻ش�������ݣ�
(2)ͼ���Ǽ����ʽȼ�ϵ�أ������Ǽ���ʧȥ���ӱ������ķ�Ӧ���ݴ�д�����缫����ʽ��
(1)��A.��Ϊ��ѧ��ת��Ϊ���ܵ�װ�ã�����û���γɱպϻ�·����A����
B.������Ҫ��п��ϡ���ᷴӦ��пƬ�ܽ⣬��пƬ����������ݣ���B��ȷ��
C.�ס����о�ΪпƬ������С��ͭƬ�������ֲ��䣬��C����
D.�������ձ������ᱻ���ģ�������Ũ�ȼ�С��pH����D��ȷ��
����BD��
����ͬ���������ձ��в���ͬ���������ʱ����Ϊ��װ����ԭ���װ�ã�����з�Ӧ���ʴ�����ʱ��Σ�����Ҫ��ʱ���С���ң�
����<��
�ۼ�Ϊԭ��أ�����Ϊп����缫��ӦʽΪ��Zn��2e��=Zn2����
����Zn��2e��=Zn2����
�ܵ�������Һ��������15.75gʱ����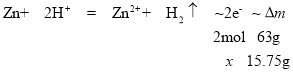 ����x=0.5mol���ʵ缫��ת�Ƶ�����ĿΪ0.5 NA��
����x=0.5mol���ʵ缫��ת�Ƶ�����ĿΪ0.5 NA��
����0.5 NA��
(2)ͨ������һ��Ϊ�����������ڼ���������ʧȥ����ת��Ϊ̼�������Ӧ�ĵ缫��ӦʽΪ![]() ��
��
����![]() ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ���Ͻ�(��������)����Ϊԭ�ϻ�������ͭ�Ĺ����������£�

����˵����ȷ����
A. ��ͭ���ڹ���ϡ���ᣬ���ˡ����¸���ô�ͭ
B. ���ʱ�ô�������������������ҺΪ�������Һ
C. ��ϡ���ᴦ������ʱ��Ҫ������������ԭ��Ӧ
D. ����ҺB�п�����ȡ�̷�(FeSO4��7H2O)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1.000mol��L��1�������20.00mL 1.000mol��L��1��ˮ�У���ҺpH���¶��������������仯��������ͼ��ʾ�������й�˵����ȷ����

A��a����ˮ�������c(H��)=1.0��10��14mol/L
B��b�㣺c(NH4��)��c(NH3��H2O) ��c(Cl��)
C��b��ʱ������������С��20.00mL����c��ʱ����������������20.00mL
D��d�����Һ�¶����½�����Ҫԭ����NH3��H2O��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��װ�ã�X��Y���Ƕ��Ե缫������Դ��ͨ���ף��е����̪��Һ����Fe�������Ժ�ɫ��������ʢ��100 mL 3.00 mol.L-1��CuSO4��Һ���Իش���������:
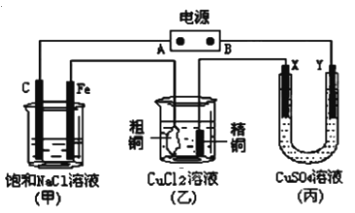
��1���ڵ�Դ�У�B�缫Ϊ ������缫���ƣ���ͬ������װ���д�ͭΪ ����
��2���ڼ�װ���У�ʯī��C���缫�Ϸ��� ��Ӧ�����������ԭ��������װ�����ܵĻ�ѧ����ʽ�� ��
��3�������װ���о�ͭ�缫������������0.64g�����ʼ�װ���У����缫�ϲ����������ڱ�״����Ϊ L��
��4���ڱ�װ���У� X�缫�Ϸ����ĵ缫��Ӧʽ�� ��
��5���ڴ˹����У������������缫����������ǡ�����ʱ�����������ҳ��о�ͭ������ g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������Һ��ʯ��������Ҫ�ɷ�֮һ�Ǽ��飬��16 kg������ȫȼ�ղ����ɶ�����̼�����Һ̬ˮʱ���ų�������Ϊ8.9��105 kJ����֪1molҺ̬ˮ����ʱ��Ҫ����44 kJ��������д������ȼ������ˮ�������Ȼ�ѧ����ʽ�� ��
��2����ͬѧ�ü��������Ϊԭ������һȼ�յ�أ�����ϡ����Ϊ�������Һʱ���为����ӦʽΪ ��
��3����֪��1 mol H��H����1 molN��H����1 molN��N���ֱ���Ҫ��������akJ��bkJ��ckJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҷ���(H2NCH2CH2NH2)����ɫҺ�壬���������ڰ���NH3+H2O![]() NH4++OH-��25��ʱ��kb1=10-4.07��kb2=10-7.15���Ҷ�����Һ�к����������ʵ���Ũ�ȷ�������ҺpH�ı仯��ͼ������˵������ȷ���ǣ� ��
NH4++OH-��25��ʱ��kb1=10-4.07��kb2=10-7.15���Ҷ�����Һ�к����������ʵ���Ũ�ȷ�������ҺpH�ı仯��ͼ������˵������ȷ���ǣ� ��
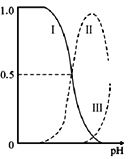
A. ���ߢ������������ΪH2NCH2CH2NH3+
B. ���ߢ�������II�ཻ���ӦpH=6.85
C. �Ҷ�����ˮ��Һ�еڶ�������ķ���ʽH2NCH2CH2NH3++H2O![]() [H3NCH2CH2NH3]2++OH-
[H3NCH2CH2NH3]2++OH-
D. 0.1 mol/LH2NCH2CH2NH3Cl��Һ�и�����Ũ�ȴ�С��ϵΪ��c(Cl-)>c(H2NCH2CH2NH3+)>c(H+)>c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(SO2Cl2)��һ����Ҫ���л��ϳ��Լ�,ʵ���ҿ�����SO2��Cl2�ڻ���̿�����·�Ӧ��ȡ������SO2Cl2,װ����ͼ��ʾ(���ּг�װ��ʡ��)����֪SO2Cl2���۵�Ϊ-54.1 �棬�е�Ϊ69.1 �棬��ˮ�ܷ������ҵ�ˮ�ⷴӦ��������������

(1)����B������Ϊ_____,������B��ʹ�ÿ�֪SO2��Cl2��Ӧ����H____(����>������<��)0��
(2)����C��������________________________________��
(3)�Լ�X��Y����������˵���______��
a.18.4mol/LH2SO4��Һ+Cu b.4mol/LHNO3��Һ+Na2SO3 c.75%H2SO4��Һ+K2SO3
(4)��Ӧ���������в�������ʵ�������������______��
(5)�����������õ�SO2Cl2�м�������NaOH��Һ�������õõ���ɫ��Һw��
��д���÷�Ӧ�����ӷ���ʽ:___________��
�ڼ�����Һw�д���SO42-�ķ�����________��
(6)����Ӧ�����ĵ����������Ϊ896 mL(��ת��Ϊ��״����SO2����)�����õ������Ļ�����3.3 g��������ȵIJ���Ϊ_________(������λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ��еڢ�A��Ԫ�صĵ��ʼ��仯�������;�㷺��
��1������Ԫ��ͬ��Ķ�����Ԫ�ص�ԭ�ӽṹʾ��ͼΪ___��
��2������Ϊ�ȡ��塢��Ԫ�طǽ�����(ԭ�ӵõ�������)�ݱ���ɵ��ж�������___(�����)��
a.Cl2��Br2��I2���۵�
b.Cl2��Br2��I2��������
c.HCl��HBr��HI�����ȶ���
d.HCl��HBr��HI������
��3����ҵ�ϣ�ͨ������ת�����Ƶ�KClO3���壺
NaCl��Һ![]() NaClO3��Һ
NaClO3��Һ![]() KClO3����
KClO3����
�����I�з�Ӧ���ܻ�ѧ����ʽ��NaCl��H2O���NaClO3�� ��___��
��II��ת���Ļ�����Ӧ������___���÷�Ӧ����������KClO3���������������������ԭ����___��
��4��һ����������ˮ��Һ��1molCl-��ClOx-(x=1��2��3��4)������(kJ)��Դ�С��ͼ��ʾ��

��D��___(�����ӷ���)��
��B��A��C��Ӧ�����ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����Һ�У����ܴ������е��������±���
������ | H����K����Al3����NH |
������ | OH����SO42����CO32����AlO2�� |
��Na2O2�������������Һ�в��ȣ�����������������ͼ��ʾ��

����˵������ȷ���ǣ�
A. ���������Һ��һ����������H����NH4+��Al3����Mg2����SO42��
B. ͼ��a��4
C. b��7��c��9
D. ����Һ����Ҫ����ɫ��Ӧ�������飬����ȷ����Һȷ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com