
【题目】以铜银合金(含少量铁)废料为原料回收银和铜的工艺流程如下:

下列说法正确的是
A. 粗铜溶于过量稀硝酸,过滤、低温干燥得纯铜
B. 电解时用粗银作阴极,硝酸银溶液为电解质溶液
C. 用稀硫酸处理渣料时主要发生了氧化还原反应
D. 从滤液B中可以提取绿矾(FeSO4·7H2O)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)已知在一定条件下发生反应:A+B=C+D,14gA和9gB恰好完全反应生成0.5molC和1gD则物质C的摩尔质量为____________;
(2)某1L混合溶液中所含离子的个数比如下表,则M离子可能为(_______)
所含离子 | NO3- | SO42- | Cu2+ | M |
个数比 | 4 | 1 | 2 | 1 |
A.Ba2+ B.Mg2+ C.Cl- D.Na+
(3)已知a g气体X2中含有b个X原子,那么c g该气体在标准状况下的体积是____________;
(4)把V L含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含b mol BaCl2的溶液,恰好使SO![]() 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为________。
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. 体系压强不再变化 D. 2v逆(X)=v正(Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学电源的叙述,错误的是( )
A. 化学电源均是根据原电池的工作原理设计的
B. 在干电池中,碳棒只起导电作用,并不参加化学反应
C. 镍镉电池不能随意丢弃的原因是镍、镉的资源有限,价格昂贵
D. 燃料电池是一种高效、环保的新型化学电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备单质硅时,主要化学反应如下:①SiO2+2C![]() Si+2CO↑;②Si+2Cl2
Si+2CO↑;②Si+2Cl2![]() SiCl4;③SiCl4+2H2
SiCl4;③SiCl4+2H2![]() Si+4HCl。下列对上述三个反应的叙述中,不正确的是
Si+4HCl。下列对上述三个反应的叙述中,不正确的是
A.①③为置换反应
B.①②③均为氧化还原反应
C.三个反应的反应物中硅元素化合价均升高
D.②为化合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,能长时间保持稳定的放电电压。其电池总反应为:3Zn + 2K2FeO4 + 8H2O![]() 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是
3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是
A. 放电时负极反应为:Zn-2e-+2OH-= Zn(OH)2
B. 充电时阳极发生氧化反应,附近溶液碱性增强
C. 充电时每转移3mol电子,阴极有1.5molZn生成
D. 放电时正极反应为:FeO42- + 3e- + 4H2O = Fe(OH)3 + 5OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的 ΔH=—99kJ·mol-1.请回答下列问题:
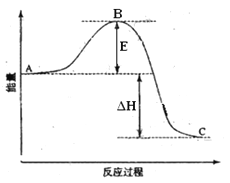
(1)图中A、C分别表示 、 ,
E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是
(2)图中△H= KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
、
;
(4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1
,则υ(O2)= mol·L-1·min-1、
υ(SO3)= mol·L-1·min-1;
(5)已知单质硫的燃烧热为296 KJ·mol-1,求由S(s)生成3 molSO3(g)的△H= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组拟设计实验探究铁盐与碳酸盐反应的产物。

对实验Ⅰ、Ⅱ反应后的混合物进行过滤洗涤、低温凉干,分别得到M、N固体。
回答下列问题
(1)用pH计分别测定0.5mol·L-1 NaHCO3溶液、0.5mol·L-1Na2CO3溶液,得pH依次为a、b。预测a___________b(填“>”“<”或“=”)
(2)为了定性确认M、N成分,进行实验:

X的化学式为___________(填化学式)
(3)为了进一步探究M(无结晶水的纯净物)的组成进行如下实验:

①点燃酒精灯前,先通入N2,其目的是____________。加热一段时间后,装置A中棕色粉末变红色,装置B中白色粉末变蓝色;装置C中产生白色沉淀。当装置A中M完全反应时停止加热,继续通入N2。
②停止加热之前,___________先拆去B、C之间导管(填“要”或“不要”)。
③对装置C中混合物进行过滤、洗涤、干燥、称重,白色固体质量为19.7g。装置A中残留红色粉末的质量为8.0g,则M的化学式为___________。
(4)FeCl3溶液和Na2CO3溶液反应的离子方程式为________。
(5)铁盐与碳酸盐溶液反应产物不同可能与___________、浓度、水解产物CO2有关。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com