
【题目】铬是一种具有战略意义的金属,它具有多种价态,单质铬熔点为1857℃。
(1)工业上以铬铁矿[主要成分是Fe(CrO2)2]为原料冶炼铬的流程如图所示:
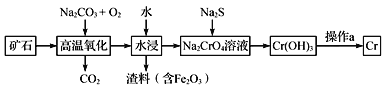
①Fe(CrO2)2中各元素化合价均为整数,则铬为_______价。
②高温氧化时反应的化学方程式为___________________________________。
(2)Cr(OH)3是两性氢氧化物,请写出其分别与NaOH、稀硫酸反应时生成的两种盐的化学式_______。
(3)铬元素能形成含氧酸及含氧酸盐,若测得初始浓度为1 mol·L-1的铬酸(H2CrO4)溶液中各种含铬元素的微粒浓度分别为:c(CrO42-)=0.0005 mol·L-1、c(HCrO4-)=0.1035 mol·L-1、c(Cr2O72-)=a mol·L-1、则a=______,KHCrO4溶液中c(OH-)______c(H+)(填“>”、“<”或“=”)。
(4)水中的铬元素对水质及环境均有严重的损害作用,必须进行无害化处理。
①处理含有Cr2O72-的污水方法通常为:用铁作电极电解污水,Cr2O72-被阳极区生成的离子还原成为Cr3+,生成的Cr3+与阴极区生成的OH结合生成Cr(OH)3沉淀除去。则阴极上的电极反应式为________________________,若要处理含10 mol Cr2O72-的污水,则至少需要消耗的铁为_______g。
②转化为重要产品磁性铁铬氧体(CrxFeyOz):先向含CrO42-的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分Fe2+)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。写出CrO42-在酸性条件下被Fe2+还原为Cr3+的离子方程式___________________。
【答案】+3 4Fe(CrO2)2+7O2+8Na2CO3![]() 2Fe2O3+8Na2CrO4+8CO2 NaCrO2、Cr2(SO4)3 0.448 < 2H2O+2e-=2OH-+H2↑(或者2H++2e-=H2↑) 3360 3Fe2++CrO42-+8H+=3Fe3++Cr3++4H2O
2Fe2O3+8Na2CrO4+8CO2 NaCrO2、Cr2(SO4)3 0.448 < 2H2O+2e-=2OH-+H2↑(或者2H++2e-=H2↑) 3360 3Fe2++CrO42-+8H+=3Fe3++Cr3++4H2O
【解析】
铬铁矿中加入碳酸钠并通入氧气,高温下将Fe(CrO2)2氧化得到Fe2O3、Na2CrO4,同时生成CO2,将得到的固体溶于水得到Na2CrO4溶液,然后过滤,向滤液中加入硫化钠,硫化钠和Na2CrO4发生氧化还原反应生成Cr(OH)3沉淀,过滤后灼烧Cr(OH)3得到Cr2O3,利用铝热反应制备金属铬,据此解答。
(1)①Fe(CrO2)2中各元素化合价均为整数,由于氧元素显-2价,铁显+2价,则根据正负价代数和为0可知铬为+3。
②高温氧化时,Fe(CrO2)2和碳酸钠、氧气发生氧化还原反应生成Na2CrO4、二氧化碳和氧化铁,该反应中Fe元素化合价由+2价变为+3价、Cr元素化合价由+3价变为+6价,O元素化合价由0价变为-2价,所以氧气是氧化剂、Fe(CrO2)2是还原剂,依据原子守恒、转移电子守恒配平后的化学方程式为4Fe(CrO2)2+7O2+8Na2CO3![]() 2Fe2O3+8Na2CrO4+8CO2。
2Fe2O3+8Na2CrO4+8CO2。
(2)Cr(OH)3是两性氢氧化物,依据氢氧化铝的性质可类推知其分别与NaOH、稀硫酸反应时生成的两种盐的化学式为NaCrO2、Cr2(SO4)3。
(3)根据Cr原子守恒可知c(CrO42-)+c(HCrO4-)+2c(Cr2O72-)=1mol/L,解得a=0.448;由于HCrO4-的电离程度大于其水解程度,则KHCrO4溶液显酸性,因此溶液中c(OH-)<c(H+)。
(4)①电解池中阴极发生得到电子的还原反应,则溶液中的氢离子在阴极放电,电极反应式为2H++2e-=H2↑。10mol Cr2O72-在反应中得到60mol电子,阳极上产生的亚铁离子就需要提供60mol电子,因此根据原子守恒可知需要铁是60mol,质量是60mol×56g/mol=3360g;
②CrO42-在酸性条件下被Fe2+还原为Cr3+,Cr元素化合价从+6价降低到+3价得到3个电子,铁元素化合价从+2价升高到+3价失去1个电子,根据得失电子守恒、原子守恒以及电荷守恒可知反应的离子方程式为3Fe2++CrO42-+8H+=3Fe3++Cr3++4H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:

回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为____________________________,基态S原子电子占据最高能级的电子云轮廓图为________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是__。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________________。

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为________形,其中共价键的类型有________种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为anm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______________________________g·cm-3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为________nm。
所形成的正八面体的体心,该正八面体的边长为________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用物质的量浓度为0.100 0 mol·L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:

(1)用标准NaOH溶液滴定时,应将标准NaOH溶液注入_______(填“甲”或“乙”)中。
(2)某学生的操作步骤如下:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴部分充满溶液;
D.取标准NaOH溶液注入碱式滴定管至“0”刻度以上 2~3 mL;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是____→___→___→___→A→___(用字母序号填写)。判断到达滴定终点的实验现象是_____________________________________
(3)右上图是碱式滴定管中液面在滴定前后的读数, c(HCl)=_______ mol·L-1。
(4)由于错误操作,使得上述所测盐酸溶液的浓度偏高的是________(填字母)。
A.中和滴定达终点时俯视滴定管内液面读数
B.酸式滴定管用蒸馏水洗净后立即取用25.00 mL待测酸溶液注入锥形瓶进行滴定
C.碱式滴定管用蒸馏水洗净后立即装标准溶液来滴定
D.用酸式滴定管量取待测盐酸时,取液前有气泡,取液后无气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若下列图像中横轴代表所加溶液体积,纵坐标代表生成沉淀质量,则各项描述中与图像能对应的是( )

A. 图①可能是MgCl2、AlCl3溶液逐滴加氨水至过量
B. 图②可能是AlCl3溶液逐滴加NaOH溶液至过量
C. 图③可能是NaAlO2溶液滴加稀盐酸至过量
D. 图④可能是含一定量HCl的AlCl3溶液逐滴加氨水至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应属于放热反应的是( )
①浓硫酸的稀释 ②工业合成氨 ③NaOH固体溶于水 ④氢氧化钡晶体与氯化铵混合 ⑤CaO溶于水 ⑥Al在高温条件下与Fe2O3的反应 ⑦酸碱中和反应
A.①②③⑤⑦B.②⑥⑦C.②⑤⑥⑦D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液流式铅蓄电池以可溶性的甲基磺酸铅[(CH3SO3)2Pb]代替硫酸作为电解质溶液,该电池充放电的总反应为2Pb2++2H2O![]() Pb+PbO2+4H+,下列说法正确的是( )
Pb+PbO2+4H+,下列说法正确的是( )
A.该电池放电时,两极质量均增加
B.放电时,正极的电极反应式为PbO2+4H++2e-![]() Pb2++2H2O
Pb2++2H2O
C.充电时,溶液中Pb2+向阳极移动
D.充电时,阳极周围溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二羟基甲戊酸是合成青蒿素的原料之一,其结构如图a所示。下列有关二羟基甲戊酸的说法正确的是

A. 含有羟基和酯基两种官能团
B. 不能使酸性KMnO4溶液褪色
C. 等量的二羟基甲戊酸消耗Na和NaHCO3的物质的量之比为3:1
D. 是乳酸(结构如图b)的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案合理的是( )
A. 配制银氨溶液:向洁净试管中加一定量AgNO3溶液后,边滴加稀氨水边摇动试管直至最初产生的沉淀恰好溶解。
B. 配制Cu(OH)2悬浊液:在一定量CuSO4溶液中,加入少量NaOH溶液
C. 制备乙酸乙酯:用右图所示的实验装置
D. 鉴别甲苯和苯:将溴的四氯化碳溶液分别滴加到少量甲苯和苯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将 NaOH 溶液滴加到 HA 溶液中,测得混合溶液的 pH 的变化关系如下图所示(已知: ![]() )。下列叙述错误的是( )
)。下列叙述错误的是( )

A. m 点:c(A-) = c(HA)
B. Ka(HA)的数量级为 10-4
C. 水的电离程度:m < r
D. r 点:c(H+) = c(A-)+c(OH-)c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com