
【题目】下列说法错误的是
A. “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
B. 水玻璃、双氧水、漂粉精、硅胶都是混合物
C. 直径在10-9 ~ 10-7mNaCl固体小颗粒分散到水中能形成胶体
D. “陶成雅器”的主要原料是黏土
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】下列关于能量变化的说法正确的是( )
A. 化学反应通常伴随着能量变化,其表现形式只有吸热和放热两种
B. 需要在高温条件下才能发生的反应一定是吸热反应
C. 因为3O2![]() 2O3是吸热反应,所以O3比O2更稳定
2O3是吸热反应,所以O3比O2更稳定
D. 吸收或放出热量的多少与参加反应的物质的多少有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,回答问题。

①A中碎瓷片的作用是___________。
②B中反应类型是______,C中实验现是____________________________。
(2)在一定条件下,乙烷和乙烯都能制得一氯乙烷(CH3CH2Cl),据此回答问题:
①方法一:由乙烷制备一氯乙烷的的化学方程式为:____________________。
方法二:由乙烯制备一氯乙烷的反应类型属于_______________。
比较以上两种方法,方法______较好,其原是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
(1)打开K2 ,合并K1 ,若所盛溶液为CuSO4溶液:则A为 极,A极的电极反应式为 。若所盛溶液为KCl溶液:则B极的电极反应式为 , K+移向 极(填A、B)

(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:①A电极附近可观察到的现象是 。
②B电极上的电极反应式为 ,总反应化学方程式是 。
③反应一段时间后打开K2 , 若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL, 将溶液充分混合,溶液的pH约为 。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的 。
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是 ,电极反应式是 ,反应一段时间后电解质溶液中Cu2+浓度 (填“增大”、“减小”、“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质之间有下图所示的转化关系.已知:A是空气中的主要成分,B、C、D均为化合物,且C为红棕色气体.
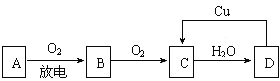
请回答下列问题:
(1)写出A和C的名称或化学式:A_________________,C________________;
(2)在上图D→C的过程中,D表现出强__________________(填“氧化性”或“还原性”);
(3)在D的稀溶液中滴入NaOH溶液,其反应的离子方程式是_________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有K+、Na+、Fe3+、Fe2+、SO42-、CO32-、I-、Cl-中的一种或多种,进行如图所示的实验,下列说法正确的是 ( )
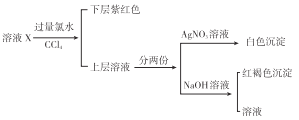
A. 溶液X中有Fe3+、SO42-
B. 溶液X中有Fe2+、I-可能有SO42-、Cl-
C. 溶液X中有I-、Cl-,无CO32-
D. 溶液X中有I-,Fe2+和Fe3+两种离子中至少有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三种有机物是某些药物中的有效成分,以下说法中正确的是( )

A. 三种有机物都能与浓溴水发生反应
B. 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种
C. 将等物质的量的三种物质加入氢氧化钠溶液中,阿司匹林消耗氢氧化钠最多
D. 只用FeCl3溶液就能鉴别出这三种有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
请回答下列问题:
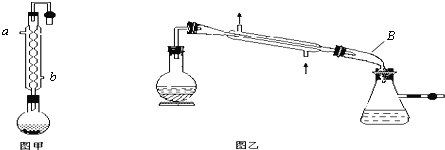
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入__________,目的是__________。
(2)反应中加入过量的乙醇,目的是__________________________。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴
加乙酸边加热蒸馏。这样操作可以提高酯的产率,其原因是____________________。
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:

则试剂a是:____________,分离方法I是____________,分离方法II是____________,
试剂b是______________,分离方法III是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
汽车尾气净化的主要原理为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
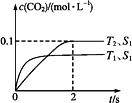
据此判断:
(1)该反应的ΔH____(填“>”或“<”)0。
(2)在T2温度下,0~2 s内的平均反应速率v(N2)=____。
(3)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。___________________
(4)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____(填代号)。
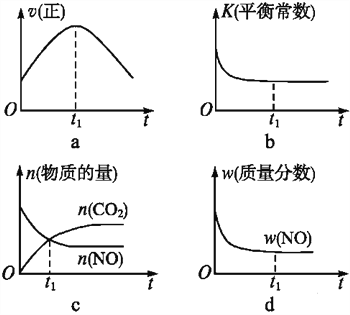
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com