
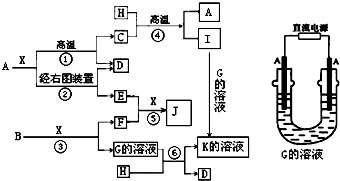
 如图表示各物质之间的转化关系,已知A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液.请按要求填空:
如图表示各物质之间的转化关系,已知A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液.请按要求填空:
| ||
| ||
| 1mol |
| 2 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A、Cu(OH)2
| ||||
| B、CO2+H2O═H2CO3 化合反应 | ||||
C、Fe2O3+3CO
| ||||
| D、NaCl+AgNO3═AgCl↓+NaNO3 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、112mL,0.04mol/L |
| B、56mL,0.02mol/L |
| C、56mL,0.04mol/L |
| D、112mL,0.02mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、34.3% |
| B、31.3% |
| C、27.3% |
| D、33.3% |
查看答案和解析>>
科目:高中化学 来源: 题型:
 小苏打长期放置在空气中会变质(部分转变为Na2CO3),某研究小组测定某小苏打样品中NaHCO3的质量分数,设计如下实验方案:
小苏打长期放置在空气中会变质(部分转变为Na2CO3),某研究小组测定某小苏打样品中NaHCO3的质量分数,设计如下实验方案:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4OH--4e-═2H2O+O2↑ |
| B、S2--2e-═S |
| C、2Cl--2e-═Cl2↑ |
| D、2Br--2e-═Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.2 mol |
| B、0.4 mol |
| C、0.6 mol |
| D、0.8 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com