
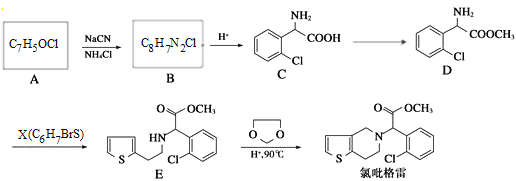
【题目】氯吡格雷(clopidogrel)是一种用于抑制血小板聚集的药物.以芳香族化合物A为原料合成的路线如下:
已知:①R-CHO![]() ,②R-CN
,②R-CN![]() RCOOH
RCOOH
(1)写出反应C→D的化学方程式______________,反应类型____________。
(2)写出结构简式.B____________,X____________。
(3)A属于芳香族化合物的同分异构体(含A)共有______种,写出其中与A不同类别的一种同分异构体的结构简式___________。
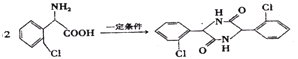
(4)两分子C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环,写出该反应的化学方程式________________。
(5)已知:![]() ,设计一条由乙烯、甲醇为有机原料制备化合物
,设计一条由乙烯、甲醇为有机原料制备化合物![]() 的合成路线流程图,无机试剂任选_____________。(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A
的合成路线流程图,无机试剂任选_____________。(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A![]() B…
B…![]() 目标产物)
目标产物)
【答案】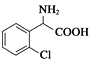 +CH3OH
+CH3OH ![]()
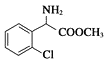 + H2O 酯化反应(或取代反应)
+ H2O 酯化反应(或取代反应) 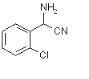
![]() 4
4 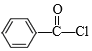
 +2H2O
+2H2O 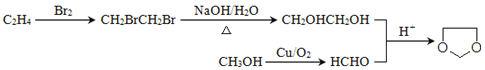
【解析】
A分子式为C7H5OCl,结合题干信息可知A中含有-CHO、-Cl、苯环,根据物质反应过程中物质结构不变,可知A为![]() ,B为
,B为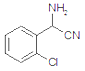 ,经酸化后反应产生C为
,经酸化后反应产生C为 ,C与甲醇在浓硫酸存在条件下加热,发生酯化反应产生D:
,C与甲醇在浓硫酸存在条件下加热,发生酯化反应产生D: ;D与分子式为C6H7BrS的物质反应产生E:
;D与分子式为C6H7BrS的物质反应产生E: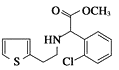 ,结合D的结构可知X结构简式为:
,结合D的结构可知X结构简式为:![]() ;E与
;E与![]() 在加热90℃及酸性条件下反应产生氯吡格雷:
在加热90℃及酸性条件下反应产生氯吡格雷: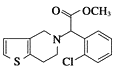 。
。
根据上述分析可知:A为![]() ,B为
,B为 ,X为:
,X为:![]() 。
。
(1)反应C→D是 与甲醇发生酯化反应,反应方程式为:
与甲醇发生酯化反应,反应方程式为: +CH3OH
+CH3OH ![]()
 + H2O,该反应为酯化反应,也属于取代反应;
+ H2O,该反应为酯化反应,也属于取代反应;
(2)根据上述分析可知B/span>为: ,X为:
,X为:![]() ;
;
(3)A结构简式为![]() ,A的同分异构体(含A)中,属于芳香族化合物,则含有苯环,官能团不变时,有邻、间、对三种,若官能团发生变化,侧链为-COCl,符合条件所有的结构简式为
,A的同分异构体(含A)中,属于芳香族化合物,则含有苯环,官能团不变时,有邻、间、对三种,若官能团发生变化,侧链为-COCl,符合条件所有的结构简式为![]() 、
、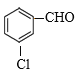 、
、![]() 、
、 ,共四种不同的同分异构体,其中与A不同类别的一种同分异构体的结构简式为
,共四种不同的同分异构体,其中与A不同类别的一种同分异构体的结构简式为 ;
;
(4)两分子C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环,应是氨基与羧基之间发生脱水反应,两分子C脱去2分子水生成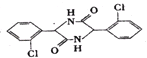 ,该反应方程式为:
,该反应方程式为: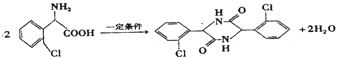 ;
;
(5)乙烯与溴发生加成反应产生CH2Br-CH2Br,再发生水解反应产生乙二醇:CH2OH-CH2OH,甲醇催化氧化产生甲醛HCHO,最后乙二醇与甲醛反应生成化合物![]() ,故该反应流程为
,故该反应流程为 。
。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】与NO2+互为等电子体的分子________,根据等电子体原理,在NO2+中氮原子轨道杂化类型是________;O22+与N2互为等电子体,1mol O22+中含有的π键数目为________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置不能完成相应实验的是
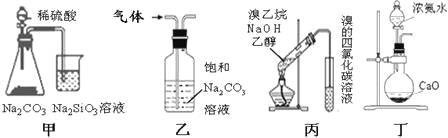
A.甲装置可比较硫、碳、硅三种元素的非金属性强弱
B.乙装置可除去CO2中少量的SO2杂质
C.丙装置可用于检验溴乙烷与NaOH的醇溶液共热产生的乙烯
D.丁装置可用于实验室制备氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼(![]() )、肼(
)、肼(![]() )和四氧化二氧(
)和四氧化二氧(![]() )可作为运载火箭的推进剂。
)可作为运载火箭的推进剂。
(1)已知:![]()
![]()
![]()
![]()
![]()
![]()
![]() 和
和![]() 反应生成
反应生成![]() 、
、![]() 和
和![]() 并放出大量热,写出该反应的热化学方程式(
并放出大量热,写出该反应的热化学方程式(![]() 用含
用含![]() 、
、![]() 、
、![]() 的代数式表示)__________。该反应______(填“是”或“不是”)自发反应,判断的理由是_______。
的代数式表示)__________。该反应______(填“是”或“不是”)自发反应,判断的理由是_______。
(2)肼(![]() )也可用于新型环保燃料电池中,燃料电池的工作原理示意图如图1所示,该燃料电池的负极反应式为_________________________________。
)也可用于新型环保燃料电池中,燃料电池的工作原理示意图如图1所示,该燃料电池的负极反应式为_________________________________。
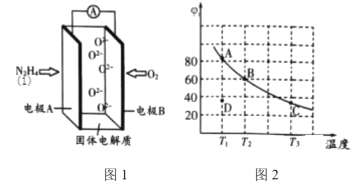
(3)将4molN2O4放入2 L,恒容密闭容器中发生反应N2O4(g) ![]() 2NO2(g),平衡体系中N2O4的体积分数(
2NO2(g),平衡体系中N2O4的体积分数(![]() )随温度的变化如图2所示
)随温度的变化如图2所示
①D点v(正)________v(逆)(填“>”“=”或“<”)。
②A、B、C点中平衡常数K的值最大的是________点。![]() 时,N2O4的平衡转化率为________;若达平衡时间为5 s,则此时间内的
时,N2O4的平衡转化率为________;若达平衡时间为5 s,则此时间内的![]() 平均反应速率为________。
平均反应速率为________。
③若其条件不变,在![]() 原平衡基础上,再加入一定量
原平衡基础上,再加入一定量![]() ,达到新平衡时,与原平衡相比,NO2的体积分数________(填“增大”“不变”或“减小”)。
,达到新平衡时,与原平衡相比,NO2的体积分数________(填“增大”“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化。
完成下列计算:
(1)将7.8克Na2O2完全溶解于93.8克水中,所得溶液的质量百分比浓度为______。
(2)将11.6克二氧化碳和水蒸汽的混合物与足量的Na2O2充分反应,固体质量增加了3.6克,则原混合气体的平均分子量为______。
(3)向100 mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M(不含结晶水)。通入二氧化碳的体积V(标准状况下)与M的质量W的关系如下图所示。
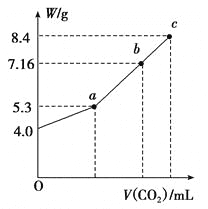
①推断b点时M的组成成份(写出计算过程)____________。
②若向b点的盐溶液中只加入0.03mol某钠的化合物,充分反应后,减压低温蒸发得到无水Na2CO3 8.48g,则加入的物质可以是________或_______。
(4)由31g NaOH和NaHCO3的固体混合物,在密闭密器中加热到250℃,经充分反应后排出气体、冷却,称得剩余固体的质量为N g,试分析不同N值时,剩余固体的组成成份(已知NaHCO3的分解温度低于250℃)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示:
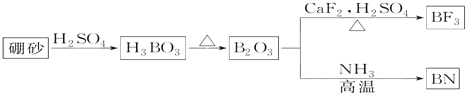
请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式是___、___。
(2)基态B原子的电子排布式为___;B和N相比,非金属性较强的是___,BN中B元素的化合价为___;
(3)在BF3分子中,F﹣B﹣F的键角是___,该分子为___分子(填写“极性” 或“非极性”),BF3和过量NaF作用可生成NaBF4,BF4-中可能含有___,立体结构为___;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为___,层间作用力为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数,但资料表明:反应中除了生成NO2气体外还会有少量的NO生成;常温下NO2和N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。为完成测定并验证确有NO生成,有人设计如下实验:
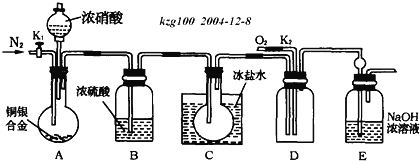
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是___。
(2)装置B瓶的作用是___。
(3)A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO产生,则D中应出现的现象是___;实验发现,通入氧气温度的高低对实验现象有较大影响,则为便于观察应通入___(填“冷”或“热”)的氧气。
(4)为减小测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是___。
(5)实验测得下列数据:所用铜银合金质量:15.0g、浓硝酸:40mL13.5mol/L;实验后A中溶液体积:40mL;H+浓度:1.0mol/L。若设反应中硝酸既无挥发也无分解,则:
①参加反应的硝酸的物质的量为___。
②若已测出反应后E装置的生成物中含氮元素的质量,则为确定合金中铜的质量分数还需要测定的数据是___。
(6)若实验只测定 Cu的质量分数,不验证NO的产生,则在铜银合金中与浓硝酸反应后,只需要简单的实验操作可达到目的,请简述实验过程:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液分别滴加到两种一元弱酸HA和HB中,两种混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是

A. 电离常数:Ka(HB)>Ka(HA)
B. Ka(HA)的数量级为10-5
C. 当HA与NaOH溶液混合至中性时:c(A-)=c(HA)
D. 等浓度等体积的HA和NaB混合后所得溶液中:c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼(B)及其化合物在化学工业中有诸多用途。请回答下列问题:
(1)硼氢化钠(NaBH4)是硼的重要化合物。
①NaBH4中B元素的化合价为___。
![]() 工业上可利用硼酸甲酯[B(OCH3)3]与氢化钠(NaH)反应制备NaBH4,反应的另一种产物为甲醇钠(CH3ONa),该反应的化学方程式为___。NaBH4与水反应生成NaBO2和H2,该反应生成的氧化产物与还原产物的物质的量之比为___。
工业上可利用硼酸甲酯[B(OCH3)3]与氢化钠(NaH)反应制备NaBH4,反应的另一种产物为甲醇钠(CH3ONa),该反应的化学方程式为___。NaBH4与水反应生成NaBO2和H2,该反应生成的氧化产物与还原产物的物质的量之比为___。
(2)工业上以铁硼矿(主要成分为Mg2B2O5·H2O,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备单质B的工艺流程如图所示:
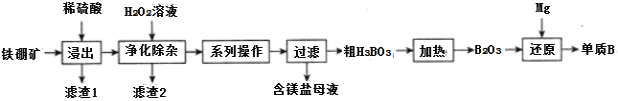
已知:
金属离子 | Fe3+ | Al3+ |
开始沉淀的PH | 2.7 | 3.1 |
沉淀完全的PH | 3.7 | 4.9 |
![]() “浸出”时,将铁硼矿石粉碎的目的为___。
“浸出”时,将铁硼矿石粉碎的目的为___。
![]() 滤渣1的主要成分为___。
滤渣1的主要成分为___。
![]() “净化除杂”时需先加H2O2溶液,其目的为___,然后再调节溶液的pH≈5.0的目的是___。
“净化除杂”时需先加H2O2溶液,其目的为___,然后再调节溶液的pH≈5.0的目的是___。
![]() 制得的粗硼在一定条件下能生成BI3,BI3加热分解可以得到纯净的单质硼。现将0.025g粗硼制成的BI3完全分解,生成的I2用0.30mol·L-1Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-)至终点,消耗18.00mLNa2S2O3溶液。盛装Na2S2O3溶液应用___(填“酸式”或“碱式”)滴定管,该粗硼样品的纯度为___。
制得的粗硼在一定条件下能生成BI3,BI3加热分解可以得到纯净的单质硼。现将0.025g粗硼制成的BI3完全分解,生成的I2用0.30mol·L-1Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-)至终点,消耗18.00mLNa2S2O3溶液。盛装Na2S2O3溶液应用___(填“酸式”或“碱式”)滴定管,该粗硼样品的纯度为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com