
□NH![]() +□O2→□NO
+□O2→□NO![]() +□H++□H2O。
+□H++□H2O。
(1)配平上面化学方程式,将化学计量数填入方框中。
(2)将铵态氮中的1 mg氮转化为硝酸根离子中的氮,需氧气多少毫克?
(3)为什么在反应中需要不断添加碱?
科目:高中化学 来源: 题型:
 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图如下:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| 含镉难溶物 | CdCO3 | CdS | Cd(OH)2 |
| 溶度积常数 | 5.2×10-12 | 3.6×10-29 | 2.0×10-16 |
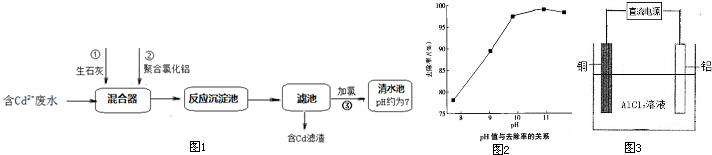
| 通电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
![]()
![]() +
+![]() O2
O2![]()
![]()
![]() +
+![]() H++
H++![]() H2O
H2O
(1)配平上面化学方程式,将化学计量数填入方框中。
(2)将铵态氮中的1 mg氮转化为硝酸根离子中的氮,需氧气多少毫克?
(3)为什么在反应中需要不断添加碱?
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com